
一定量的乙醇在氧气不足的情况下燃烧,得CO、CO2和水的总质量为27.6 g,若生成水的质量为10.8 g,则CO的质量为( )
A.1.4 g B.2.2 g
C.4.4 g D.在2.2 g和4.4 g之间
 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源:2015-2016学年江西金溪一中高一下第二次月考化学试卷(解析版) 题型:简答题
(一)已知断裂1mol C—H键,要吸收热量414.4 kJ;断裂1 mol C—C键,要吸收热量347.4 kJ;生成1 mol C===C键,会放出热量615.3 kJ;生成1 mol H—H键,会放出热量435.3 kJ。某有机物分解的反应可表示为:

若在反应中消耗了1 mol乙烷,则有关该反应的说法正确的是
A.该反应放出251.2 kJ的热量
B.该反应吸收251.2 kJ的热量
C.该反应放出125.6 kJ的热量
D.该反应吸收125.6 kJ的热量
(二)如图所示的原电池,一段时间后某极析出1.28g的固体。回答下列问题:
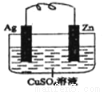
(1)正极是 (填“锌”或“银”),发生了 反应。
(2)正极的电极反应为 。
(3)上述过程中共转移电子 mol。
(4)锌片的质量 (填“增加”或“减少”) g。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年重庆一中高一下学期期中化学试卷(解析版) 题型:实验题
氧化铁是重要工业颜料,以废铁屑为原料制备氧化铁的步骤如下:(部分操作和条件略)
步骤1:用碳酸钠溶液洗去铁屑表 面的油污。
面的油污。
步骤2:加入稍过量的稀硫酸,保持50~80℃,充分反应后,过滤。
步骤3:将滤液与稍过量的NH4HCO3溶液混合,得到FeCO3的浊液。
步骤4: 、 、 ,得到FeCO3固体。
步骤5:煅烧FeCO3,得到Fe2O3固体。
(1)步骤2中,如何判断反应已经充分? 。
(2)步骤2所得的滤渣中主要含有一种铁的化合物W(Fe3C),经以下处理后,回收利用:W在足量的空气中高温煅烧,生成有磁性的固体X;将X溶于稀硫酸。
①煅烧时1 mol W消耗O2 mol。
②X溶于稀硫酸的离子方程式为 。
(3)步骤3生成FeCO3反应的化学方程式为 。
(4)将步骤4补充完整: 、 、 。
(5)若煅烧时条件控制不当,会使产品中存在杂质FeO。
①若要设计实验检验产品中是否存在FeO,且只能选用两种试剂,这两种试剂是 。
②现煅烧116.0 kg的FeCO3,得到79.2 kg产品,则该产品的纯度为__________。(设产品中只有一种杂质FeO,计算结果保留3位有效数字)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年重庆一中高一下学期期中化学试卷(解析版) 题型:选择题
下列各组大小关系比较中错误的
A.热稳定性:Na2CO3>NaHCO3 B.酸性:H2CO3>HClO
C.氧化性:浓硝酸>稀硝酸 D.结合OH- 的能力:NH4+>Al3+
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高一下第三次月考化学试卷(解析版) 题型:实验题
实验室合成乙酸乙酯的步骤如下:在圆底烧瓶内加入乙醇、浓硫酸和乙酸,瓶口竖直安装通有冷却水的冷凝管(使反应混合物的蒸气冷凝为液体流回烧瓶内),加热回流一段时间后换成蒸馏装置进行蒸馏,(如下图所示)得到含有乙醇、乙酸和水的乙酸乙酯粗产品。
请回答下列问题:(已知:乙醇、乙酸、乙酸乙酯的沸点依次是78.4℃、118℃、77.1℃)
(1)在烧瓶中除了加入乙醇、浓硫酸和乙酸外,还应放入碎瓷片,目的是 。
(2)在烧瓶中加入一定比例的乙醇和浓硫酸的混合液的方法是: 。
(3)在该实验中,若用1mol乙醇和1mol 乙酸在浓硫酸作用下加热,充分反应,能够生成1mol乙酸乙酯? ,原因是 。
(4)现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,下图是分离操作步骤流程图。请在图中圆括号内填入适当的试剂,在方括号内填入适当的分离方法。
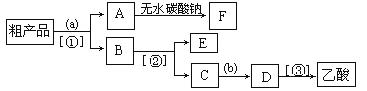
试剂a是_ __;试剂b是 ;分离方法①是______________,分离方法②是 _______,分离方法③是_______________。
(5)在得到的A中加入无水碳酸钠粉末,振荡,目的是 。
(6)写出C→D反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高一下第三次月考化学试卷(解析版) 题型:选择题
柠檬烯是一种食用香料,其结构简式如图。有关柠檬烯的分析正确的是( )
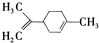
A.它的一氯代物有6种
B.它和丁基苯(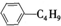 )互为同分异构体
)互为同分异构体
C.它的分子中所有的碳原子一定在同一平面上
D.一定条件下,它分别可以发生加成、取代、氧化、还原反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高一下第三次月考化学试卷(解析版) 题型:选择题
将盛有NH4HCO3粉末的小烧杯放入盛有少量醋酸的大烧杯中。然后向小烧杯中加入盐酸,反应剧烈,醋酸逐渐凝固。由此可见( )
A.NH4HCO3和盐酸的反应是放热反应
B.该反应中,热能转化为产物内部的能量
C.反应物的总能量高于生成物的总能量
D.反应的热化学方程式为NH4HCO3+HCl=NH4Cl+CO2↑+H2O ΔH=+Q kJ/mol
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川成都七中高一下甲烷课后作业化学试卷(解析版) 题型:选择题
(双选)两种气态烃以任意比例混合,在105℃ 时,1L该混合烃与9L氧气混合,充分燃烧后恢复到原状态,所得气体体积仍是1OL,下列各组混合烃中不符合此条件的是( )
A.CH4、C2H4 B.CH4、C3H6 C.C2H4、C3H4 D.C2H2、C3H6
查看答案和解析>>
科目:高中化学 来源:2016届贵州省高三押题卷理综化学试卷(解析版) 题型:选择题
已知电离平衡常数:H2CO3>HClO>HCO3-,氧化性:HClO>Cl2>Br2>Fe3+>I2。下列有关离子反应或离子方程式的叙述中,正确的是( )
A.向0.1molFeI2溶液中滴加少量 氯水,反应中有0.3NA电子转移
氯水,反应中有0.3NA电子转移
B.向溴水中加入足量氯化亚铁能使溶液变成无色
C.向NaClO溶液中通入少量CO2的离子方程式:2ClO-+CO2+H2O=2HClO+CO32-
D.能使pH试纸显深红色的溶液,Fe3+、Cl-、Ba2+、Br-能大量共存
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com