
向100mL0.1mol·L–1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1mol·L—1Ba(OH)2溶液。随着Ba(OH)2溶液体积(V)的变化,沉淀总物质的量(n)的变化如图所示。

下列叙述正确的是
A.a点的沉淀总物质的量为0.03mol
B.Oa段发生反应的离子方程式是:Al3++2SO42—+2Ba2++3OH–== Al(OH)3↓+2BaSO4↓
C.ab段发生反应的离子方程式是:2NH4++SO42—+Ba2++2OH–== 2NH3·H2O+BaSO4↓
D.反应到c点时,加入Ba(OH)2溶液的总体积为250mL
CD
【解析】
试题分析:100mL0.1mol?L-1硫酸铝铵[NH4Al(SO4)2],NH4Al(SO4)2物质的量为0.01mol.溶液含有NH4+0.01mol,Al3+0.01mol,SO42-0.02mol,反应顺序为,开始滴加同时发生反应为SO42-+Ba2+=BaSO4↓,Al3++3OH-=Al(OH)3↓,当Al3+沉淀完全时需加入0.03molOH-,即加入0.015molBa(OH)2,加入的Ba2+为0.015mol,SO42-未完全沉淀,此时溶液含有硫酸铵、硫酸铝;再滴加Ba(OH)2,生成BaSO4沉淀,发生反应为SO42-+Ba2+=BaSO4↓,NH4++OH-=NH3?H2O,所以沉淀质量继续增加,但增加幅度较前一过程小;当SO42-完全沉淀时,共需加入0.02molBa(OH)2,加入0.04molOH-,Al3+反应掉0.03molOH-,生成Al(OH)30.01mol,剩余0.01molOH-恰好与NH4+完全反应,此时溶液中NH4+完全反应,此时溶液为氨水溶液,沉淀达最大为BaSO4和Al(OH)3;继续滴加Ba(OH)2,Al(OH)3溶解,发生反应Al(OH)3+OH-=AlO2-+2H2O,由方程式可知要使0.01molAl(OH)3完全溶解,需再加入0.005molBa(OH)2,此时溶液为氨水与偏铝酸钡溶液。A、由分析可知,从开始到a点,发生反应为SO42-+Ba2+=BaSO4↓,Al3++3OH-=Al(OH)3↓,a点对应的沉淀为BaSO4和Al(OH)3,A错误;B. Oa段发生反应的离子方程式是:2Al3++3SO42—+3Ba2++6OH–== 2Al(OH)3↓+3BaSO4↓,B错误;C、由分析可知,ab断发生反应为2NH4++SO42—+Ba2++2OH–== 2NH3·H2O+BaSO ,C正确;D、由分析可知,c点加入Ba(OH)2的物质的量为0.005mol+0.02mol=0.025mol,所以0.025/0.1=0.25L=250ml,D正确;选CD。
考点:考查离子反应,离子方程式,化学反应的计算。


科目:高中化学 来源:2014-2015学年陕西省高三上学期第二次模考试化学试卷(解析版) 题型:选择题
下列说法错误的是
A.碳、硫单质在加热条件下都能与浓硝酸、浓硫酸发生反应
B.氮氧化物、二氧化硫是形成酸雨的主要物质
C.二氧化硫具有还原性,因此二氧化硫不能用浓硫酸干燥
D.硅在自然界中主要以氧化物和硅酸盐的形式存在
查看答案和解析>>
科目:高中化学 来源:2014-2015学年辽宁省高三上学期期中化学试卷(解析版) 题型:选择题
某种飞船以N2H4和N2O4为动力源,发生反应:2N2H4+N2O4===3N2+4H2O,反应温度可达2 700 ℃,对于该反应,下列说法正确的是
A.该反应属于置换反应
B.N2H4是氧化剂
C.N2O4发生氧化反应
D.氧化产物与还原产物的质量比为2:1
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省赣州市十二县高三上学期期中化学试卷(解析版) 题型:选择题
下列指定反应的离子方程式正确的是
A.向苯酚钠溶液中通入少量的CO2:C6H5O-+CO2+H2O → C6H5OH+HCO3-
B.FeS固体放入稀硝酸溶液中:FeS+2H+= Fe2++H2S↑
C.(NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH- =Fe(OH)2↓
D.用惰性电极电解氯化钠溶液:2Cl-+2H+ H2↑+Cl2↑
H2↑+Cl2↑
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省泰州市姜堰区高三上学期期中化学试卷(解析版) 题型:填空题
(20分)三氯化铬是化学合成中的常见物质,三氯化铬易升华,在高温下能被氧气氧化。制备三氯化铬的流程如下图所示:

(1)重铬酸铵分解产生的三氧化二铬(Cr2O3难溶于水)需用蒸馏水洗涤,如何用简单方法判断其已洗涤干净? 。
(2)已知CCl4沸点为76.8℃,为保证稳定的CCl4气流,适宜的加热方式是 。
(3)用下图装置制备CrCl3时,

反应管中发生的主要反应为: Cr2O3+3CCl4==2CrCl3+3COCl2,则向三颈烧瓶中通入N2的作用为:
① ;
② 。
(4)样品中三氯化铬质量分数的测定:称取样品0.3000g,加水溶解并定容于250mL容量瓶中。移取25.00mL于碘量瓶(一种带塞的锥形瓶)中,加热至沸后加入1g Na2O2,充分加热煮沸,适当稀释,然后加入过量2mol·L–1H2SO4至溶液呈强酸性,此时铬以Cr2O72–存在,再加入1.1g KI,加塞摇匀,充分反应后铬以Cr3+存在,于暗处静置5min后,加入1mL指示剂,用0.0250mol·L–1标准Na2S2O3溶液滴定至终点,平行测定三次,平均消耗标准Na2S2O3溶液21.00mL。(已知:2Na2S2O3+I2 == Na2S4O6+2NaI)
①滴定实验可选用的指示剂名称为 ,判定终点的现象是 ;若滴定时振荡不充分,刚看到局部变色就停止滴定,则会使样品中无水三氯化铬的质量分数的测量结果 (填“偏高”“偏低”或“无影响”)。
②加入Na2O2后要加热煮沸,其主要原因是 。
③加入KI时发生反应的离子方程式为 。
④样品中无水三氯化铬的质量分数为 。(结果保留一位小数)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省泰州市姜堰区高三上学期期中化学试卷(解析版) 题型:选择题
液体燃料电池相比于气体燃料电池具有体积小等优点。一种以液态肼(N2H4)为燃料的电池装置如图所示,

该电池用空气中的氧气作为氧化剂,KOH溶液作为电解质溶液。下列关于该电池的叙述正确的是
A.b极发生氧化反应
B.a极的反应式:N2H4+4OH–-4e-== N2↑+4H2O
C.放电时,电流从a极经过负载流向b极
D.其中的离子交换膜需选用阳离子交换膜
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省泰州市姜堰区高三上学期期中化学试卷(解析版) 题型:选择题
下列有关物质的性质与应用相对应的是
A.稀硝酸具有氧化性,可用于清洗做银镜反应的试管
B.BaSO4、BaCO3均难溶于水,都可用作钡餐
C.铝合金的大量使用归功于人们能用焦炭等还原剂从氧化铝中获取铝
D.加热盛有NH4Cl固体的试管,管口有固体凝结,这是升华现象
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
正确掌握好化学用语是学好化学的基础,下列化学用语正确的是
A.二氧化碳的电子式为: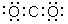 |
| B.乙烯的结构简式为:CH2CH2 |
| C.乙醇的分子式为:C2H6O |
D.Cl-离子的结构示意图为: |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
“物质的量”是指( )
| A.物质的质量 |
| B.物质的微观粒子数 |
| C.物质的质量与微观粒子数 |
| D.能把物质的质量同微观粒子数联系起来的一个基本物理量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com