
 )
)| A.Na2CO3 、NaCl 、NaOH | B.NaCl 、Na2CO3 、NaOH |
| C.NaOH 、NaCl 、Na2CO3 | D.NaCl 、NaOH 、Na2CO3 |
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案科目:高中化学 来源:不详 题型:单选题
| A.标准状况下,pH=7的醋酸和醋酸钠的混合溶液中,c(CH3COO-)=c(Na+) |
| B.pH相同的NH4Cl溶液和硫酸溶液,稀释相同倍数后,硫酸溶液的pH小 |
| C.Ba(NO3)2溶液可以鉴别SO2气体和CO2气体 |
| D.向足量饱和石灰水中加入0.56 gCaO,可析出0.74 gCa(OH)2固体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
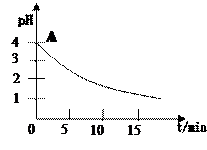
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.OH─、Al3+、SO42-、Na+ | B.Na+、NO3-、SO42-、K+ |
| C.Cl─、Ag+、H+、NO3─ | D.H+、CO32-、K+、Cl─ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在碱性溶液中:CO32—、K+、C1—、Na+ |
| B.与铝粉反应放出氢气的无色溶液中:NO3—、Mg2+、Na+、SO42— |
| C.在c(H+)/c(OH—)==1×10—12的溶液中:NH4+、Ca2+、C1—、K+ |
| D.在中性溶液中:Fe3+、Na+、SCN—、C1— |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Na+、Al3+、SO42-、NO3- | B.Ba2+、Na+、SO42-、NO3- |
| C.K+、Mg2+、MnO4-、SO42- | D.K+、Na+、NO3-、HCO3- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.CO32- | B.NO3-、 SO42- | C.CO32-、 NO3- | D.CO32- 、 SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com