
【题目】不属于NO3-的等电子体的是
A.NO2 B.BF3 C.SO3 D.NF32+
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】实验室需要0.1 mol·L-1 NaOH溶液450 mL和0.5 mol·L-1硫酸溶液500mL。根据这两种溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是①______________(填序号),配制上述溶液还需用到的玻璃仪器是②____________(填仪器名称)。
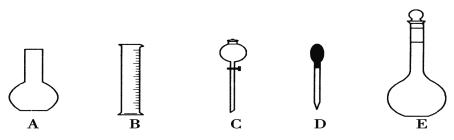
(2)根据计算用托盘天平称取NaOH的质量为③________g。在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度④__________0.1 mol·L-1(填“大于”、“等于”或“小于”)。
(3)由计算知,所需质量分数为98%、密度为1.84 g·cm-3的浓硫酸的体积为⑤________mL(计算结果保留一位小数)。如果实验室有15 mL、20 mL、50 mL量筒,应选用⑥________mL量筒最好。配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是将浓硫酸沿烧杯壁缓缓倒入水中,并用玻璃棒不断搅拌。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以NaCl等为原料制备KClO4的过程如下:
①在无隔膜、微酸性条件下,发生反应:NaCl+H2O—NaClO3+H2↑(未配平)
②在NaClO3溶液中加入KCl发生复分解反应,降温结晶,得KClO3。
③一定条件下反应:4KClO3=3KClO4+KCl,将产物分离得到KClO4。

(1)电解时,产生质量为2.13g NaClO3,同时得到H2的体积为________L(标准状况)。
(2)向NaClO3溶液中加入KCl能得到KClO3的原因是______________。
(3)该过程制得的KClO4样品中含少量KCl杂质,为测定产品纯度进行如下实验:
准确称取5.689g样品溶于水中,配成250mL溶液,从中取出25.00mL于锥形瓶中,加入适量葡萄糖,加热使ClO4-全部转化为Cl-(反应为:3 KClO4 +C6H12O6 ═ 6 H2O + 6 CO2↑ + 3 KCl),加入少量K2CrO4溶液作指示剂,用0.20mol/L AgNO3溶液进行滴定至终点,消耗AgNO3溶液体积21.00mL。滴定达到终点时,产生砖红色Ag2CrO4沉淀。
①已知: Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=1.1×10-12,若c(CrO42-)=1.1×10-4mol/L,则此时c(Cl-)=__________mol/L。
②计算KClO4样品的纯度(请写出计算过程。)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海带中含有丰富的碘。经测定:1000g某海带样品中含有6.35g碘离子。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
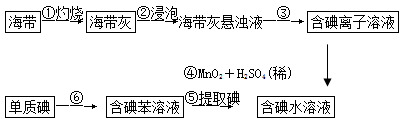
请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是 (从下列仪器中选出所需的仪器,将标号字母填写在空白处)。
A.烧杯
B.坩埚
C.表面皿
D.泥三角
E.酒精灯
F.干燥器
(2)步骤③的实验操作名称是 ;步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是
(3)步骤④反应的离子方程式是_
(4)步骤⑤中,某学生选择用苯来提取碘的理由是
(5)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法:
(6)从含碘单质的有机溶液中分离出单质碘和回收有机溶剂,应选择的实验装置是
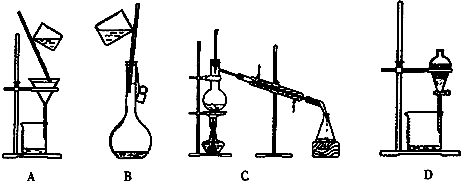
(7)若将l000g上述海带中的碘离子全部氧化,至少需要通入标准状况下的氯气的体积为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是
A.离子晶体在熔化状态下一定能导电
B.分子晶体的状态变化只需克服分子间作用力
C.金属键的本质是金属离子与自由电子间的相互作用
D.原子晶体中只存在非极性共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的。某学校课外兴趣小组从海水晒盐后的盐卤(主要含Na+、Mg2+、Cl-、Br-等)中模拟工业生产来提取镁,主要过程如下:
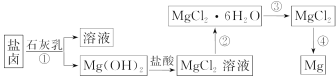
回答下列问题:
(1)工业上从盐卤中获取Mg(OH)2用石灰乳而不用NaOH溶液的原因是___ __ __ __ __ ___。
(2)从过程①得到的Mg(OH)2沉淀中混有少量的Ca(OH)2,除去少量Ca(OH)2的方法是先将沉淀加入到盛有__ ___ _溶液(填写化学式)的烧杯中,充分搅拌后经__ _ __ _ __、__ _ __ __ __(填操作方法)可得纯净的Mg(OH)2。
(3)下图是该兴趣小组设计进行过程③的实验装置图:

其中装置A的作用是___ ___ __ _ __ __ ___ __ __。
(4)写出过程④中发生反应的化学方程式___ __ __ __ __ ___。
(5)金属Mg在CO2中完全燃烧生成MgO和C,下列说法正确的是___ ___。
A.碳单质只存在金刚石和石墨两种同素异形体
B.Mg、MgO中镁元素微粒半径:r(Mg2+) > r(Mg)
C.在该反应条件下,Mg的还原性强于C的还原性
D.该反应中化学能全部转化为热能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物是药物生产的中间体,其结构简式如图。下列有关叙述不正确的是( )
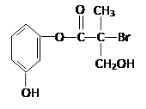
A.该有机物与浓溴水可发生取代反应
B.1 mol该有机物与足量NaOH溶液反应最多消耗4 mol NaOH
C.该有机物与浓硫酸混合共热可发生消去反应
D.该有机物经催化氧化后与新制氢氧化铜悬浊液共热生成砖红色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分子式为C8H8O3的芳香族化合物有多种不同的结构,这些物质有广泛用途。
(1)C8H8O3的某一同分异构体尼泊金酯的结构简式为:![]() 。
。
①下列对尼泊金酯的判断错误的是 。
a.能发生水解反应
b.能与FeCl3溶液发生显色反应
c.分子中所有原子都在同一平面上
d.能与浓溴水反应产生白色沉淀。
②尼泊金酯与足量NaOH溶液在一定条件下反应的化学方程式是 。
(2)C8H8O3的另一种同分异构体甲的结构简式为:![]() 。
。
①甲中含氧官能团的名称为:羧基和 。
②甲在一定条件下跟足量的Na反应的化学方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com