
����Ŀ��������ʵ��С���ͬѧΪ̽�������������������ķ�Ӧ����������ͼ��ʾ��װ�ý���ʵ�飮ͨ��SO2���壬���������ľ�������Թ�C�У�ľ����ȼ����ش��������⣺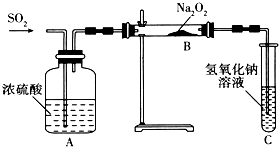
��1����1С��ͬѧ��ΪNa2O2��SO2��Ӧ������Na2SO3��O2 �� �÷�Ӧ�Ļ�ѧ����ʽ�� ��
��2�������һ��ʵ�鷽��֤��Na2O2��SO2��Ӧ���ɵİ�ɫ�����к���Na2SO3 �� ��
��3����2С��ͬѧ��ΪNa2O2��SO2��Ӧ��������Na2SO3��O2�⣬����Na2SO4���ɣ�Ϊ�����Ƿ���Na2SO4���ɣ�������������·�������B�з�Ӧ��Ĺ����ܽ���ˮ ![]() ��ɫ����
��ɫ���� ![]() ���в��ְ�ɫ�������ܽ⣬֤����Na2SO4����
���в��ְ�ɫ�������ܽ⣬֤����Na2SO4����
���������Ƿ������ �� ���Ҫ˵���������ɣ�
������ ��
���𰸡�
��1��2Na2O2+2SO2=2Na2SO3+O2
��2��ȡ��ɫ���壬��ϡ���ᣬ������ʹƷ����Һ��ɫ������
��3����������ϡ�����ܽ������ᱵ����Ϊ���ᱵ�������Ӧ��Ĺ����л�����Na2O2 �� ������ˮ���ܽ���������������������������
���������⣺��1��Na2O2��SO2��Ӧ������Na2SO3��O2 �� �÷�Ӧ�Ļ�ѧ����ʽ��2Na2O2+2SO2=2Na2SO3+O2 �� ���Դ��ǣ�2Na2O2+2SO2=2Na2SO3+O2����2��֤��Na2O2��SO2��Ӧ���ɵİ�ɫ�����к���Na2SO3 �� ʵ�鷽��Ϊȡ��ɫ���壬��ϡ���ᣬ������ʹƷ����Һ��ɫ�����壬���Դ��ǣ�ȡ��ɫ���壬��ϡ���ᣬ������ʹƷ����Һ��ɫ�����壻��3��B�з�Ӧ��Ĺ����ܽ���ˮ ![]() ��ɫ����
��ɫ���� ![]() ���в��ְ�ɫ�������ܽ⣬����֤����Na2SO4���ɣ��÷��������������ϡ�����ܽ������ᱵ����Ϊ���ᱵ���������Ӧ��Ĺ����л�����Na2O2 �� ������ˮ���ܽ��������������������������ӣ����Դ��ǣ���������ϡ�����ܽ������ᱵ����Ϊ���ᱵ�������Ӧ��Ĺ����л�����Na2O2 �� ������ˮ���ܽ��������������������������ӣ�
���в��ְ�ɫ�������ܽ⣬����֤����Na2SO4���ɣ��÷��������������ϡ�����ܽ������ᱵ����Ϊ���ᱵ���������Ӧ��Ĺ����л�����Na2O2 �� ������ˮ���ܽ��������������������������ӣ����Դ��ǣ���������ϡ�����ܽ������ᱵ����Ϊ���ᱵ�������Ӧ��Ĺ����л�����Na2O2 �� ������ˮ���ܽ��������������������������ӣ�


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йع���ϵ�˵������ȷ����( )
A. ����������õİ뵼����Ϻ�����̫���ܵ�صIJ���
B. SiO2������������ά
C. ��ͨ�������Դ��ʯ��ʯ��ʯӢΪԭ�Ͼ������ս���Ƴɵ�
D. SiO2�������������������ˮ���ɹ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ��������ܱ������з���20L����P��37L����W�� ��һ�������·�����Ӧ��3P(g)+4W(g) = 4R(g)+nY(g)��Ӧ��ȫ�������¶Ȳ��䣬��������ѹǿ��ԭ����92.5%����ѧ����ʽ�е�nֵ��
A. 3 B. 2 C. 5 D. 4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б仯�б�����뻹ԭ������ʵ�ֵ��ǣ� ��
A. HCl��Cl2B. MnO4-��Mn2+C. KClO3��O2D. Fe��Fe2+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��һ��ӦΪ��3Fe2++2S2O32-+O2+xOH-�TFe3O4+S4O62-+2H2O������˵���в���ȷ���ǣ�������
A. x=4
B. 1mol Fe2+������ʱ����Fe2+��ԭ��O2�����ʵ���Ϊ1/3 mol
C. Fe2+��S2O32-���ǻ�ԭ��
D. ÿ����1mol Fe3O4����Ӧת�Ƶ��ܵ�����Ϊ4mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������֯(WHO)����������(ClO2)��ΪA����Ч��ȫ���������������ʳƷ���ʡ�����ˮ�����ȷ������Ź㷺Ӧ�ã��ɴ˿��ж϶�������()
A.��ǿ������
B.��ǿ��ԭ��
C.�����ӻ�����
D.��������Ԫ��Ϊ��1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʲ���ʹ��īˮ��ɫ����(����)
A. ����̿B. ��������C. NaCl��ҺD. Ư��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1200��ʱ����Ȼ���������лᷢ�����з�Ӧ��
H2S��g��+O2��g���TSO2��g��+H2O��g����H1
2H2S��g��+SO2��g���TS2��g��+2H2O��g����H2
H2S��g��+O2��g���TS��g��+H2O��g����H3
2S��g���TS2��g����H4
���H4����ȷ����ʽΪ�� ��
A.��H4= ![]() ����H1+��H2��3��H3��
����H1+��H2��3��H3��
B.��H4= ![]() ��3��H3����H1����H2 ��
��3��H3����H1����H2 ��
C.��H4= ![]() ����H1+��H2��3��H3��
����H1+��H2��3��H3��
D.��H4= ![]() ����H1����H2��3��H3��
����H1����H2��3��H3��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com