
【题目】设NA代表阿伏加德罗常数,下列说法正确的是( )
A.4.6gNa完全转化成Na2O和Na2O2的混合物,生成物中阴离子总数为0.1NA
B.标准状况下,22.4L丙烷所含共用电子对数为8NA
C.标准状况下,2.24LCl2溶于水,转移的电子数目为0.1NA
D.常温下,1L0.1mol·L-1NH4NO3溶液中含有的NH4+数是0.1NA
【答案】A
【解析】
A.氧化钠和过氧化钠中阴阳离子个数比都是1∶2,4.6g钠的物质的量是0.2mol,4.6gNa完全转化成Na2O和Na2O2的混合物,钠离子的物质的量是0.2mol,所以生成物中阴离子为0.1mol,阴离子总数为0.1 NA,故A正确;
B.标准状况下,22.4L丙烷的物质的量为![]() =1mol,C3H8含共用电子对数=1mol×10×NA=10NA,故B错误;
=1mol,C3H8含共用电子对数=1mol×10×NA=10NA,故B错误;
C.氯气和水的反应为可逆反应,不能完全反应,故转移的电子数小于0.1NA个,故C错误;
D.铵根离子能少量水解,1L0.1mol·L-1NH4NO3溶液中含有铵根离子的数目小于0.1NA,故D错误;
故选A。


科目:高中化学 来源: 题型:
【题目】用H2O2、KI和洗洁精可完成“大象牙膏”实验(短时间内产生大量泡沫),某同学依据文献资料对该实验进行探究。
(1)资料1:KI在该反应中的作用:
H2O2+I-=H2O+IO-;H2O2+IO-=H2O+O2↑+I-。总反应的化学方程式是________________。
(2)资料2:H2O2分解反应过程中能量变化如图所示,其中①有KI加入,②无KI加入。下列判断正确的是___________(填字母)。
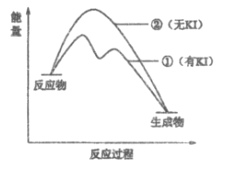
a. 加入KI后改变了反应的路径
b. 加入KI后改变了总反应的能量变化
c. H2O2+I-=H2O+IO-是放热反应
(3)实验中发现,H2O2与KI溶液混合后,产生大量气泡,溶液颜色变黄。再加入CCl4,振荡、静置,气泡明显减少。
资料3:I2也可催化H2O2的分解反应。
①加CCl4并振荡、静置后还可观察到___________,说明有I2生成。
②气泡明显减少的原因可能是:i. H2O2浓度降低;ii. ________。以下对照实验说明i不是主要原因:向H2O2溶液中加入KI溶液,待溶液变黄后,分成两等份于A、B两试管中。A试管加入CCl4,B试管不加CCl4,分别振荡、静置。观察到的现象是_____________。
(4)资料4:I-(aq)+I2(aq)![]() I3-(aq) K=640。
I3-(aq) K=640。
为了探究体系中含碘微粒的存在形式,进行实验:向20 mL一定浓度的H2O2溶液中加入10mL 0.10mol·L-1 KI溶液,达平衡后,相关微粒浓度如下:
微粒 | I- | I2 | I3- |
浓度/(mol·L-1) | 2.5×10-3 | a | 4.0×10-3 |
①a=__________。
②该平衡体系中除了含有I-,I2,I3-外,一定还含有其他含碘微粒,理由是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)如图进行实验,将a溶液逐渐加入盛b溶液的试管中,写出试管中观察到的现象及对应的离子方程式___。
a | b | 试管中现象 | 离子方程式 |
Na2CO3 | 稀盐酸 | ||
稀盐酸 | Na2CO3 |
(2)工业上利用NaIO3和NaHSO3反应来制取单质I2。配平下列化学方程式并用单线桥法表示电子转移的方向和数目:___。
NaIO3+NaHSO3=I2+Na2SO4+H2SO4+H2O
(3)ClO2常用于水的净化,工业上可用Cl2氧化NaClO2溶液制取ClO2。写出该反应的离子方程式,并用双线桥法表示电子转移的方向和数目___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在反应2A+B3C+4D中,表示该反应速率最快的是( )
A.v(A)=0.5 mol·L-1·s-1B.v(B)=0.3 mol·L-1·s-1
C.v(C)=48 mol·L-1·min-1D.v(D)=10 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用燃烧法测定某种氨基酸(CxHyOzNm)的分子组成。取Wg该种氨基酸放在纯氧中充分燃烧,生成二氧化碳、水和氮气。按下图所示装置进行实验。

回答下列问题:
(1)实验开始时,首先通入一段时间的氧气,其理由是__________________。
(2)以上装置中需要加热的仪器有_______ (填写字母),操作时应先点燃_____处的酒精灯。
(3)A装置中发生反应的化学方程式是____________________________。
(4)D装置的作用是____________________________。
(5)读取氮气的体积时,应注意①_________________;②_________________。
(6)实验中测得氮气的体积为VmL(标准状况),为确定此氨基酸的分子式,还需要的有关数据有____________________。
A.生成二氧化碳气体的质量
B.生成水的质量
C.通人氧气的体积
D.氨基酸的相对分子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关Na2CO3和NaHCO3性质的出较中,正确的是
A. 等浓度的溶液中滴入稀盐酸,放出气体的快慢Na2CO3<NaHCO3
B. 热稳定性Na2CO3<NaHCO3
C. 常温时水溶性Na2CO3<NaHCO3
D. 可以用澄清石灰水鉴别Na2CO3和NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋中有丰富的食品、矿产、能源、药物和水产资源等(如图所示)。

下列有关说法正确的是( )
A.大量的氮、磷废水排入海洋,易引发赤潮
B.在③中加入盐酸溶解得到MgCl2溶液,再直接蒸发得到MgCl2·6H2O
C.在④⑤⑥中溴元素均被氧化
D.在①中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组用如下图所示装置A、B分别探究金属铝与稀氢氧化钠溶液的反应,实验过程中装置A中烧杯内的溶液温度升高,装置B中烧杯的电流计指针发生偏转,请回答以下问题。

(1)装置A烧杯中反应的离子方程式为_________。
(2)装置B中Mg上的现象是_________,Al发生的电极反应式是__________________。
(3)当装置B导线中通过0.3mol电子时,装置B烧杯中溶液的质量变化为__________(填增重或减轻多少克)。
(4)该小组同学反思原电池的原理,其中观点正确的是_________(填字母序号)。
A.原电池反应的过程中一定有电子转移
B.原电池装置需要2个电极
C.电极一定不能参加反应
D.氧化反应和还原反应可以拆开在两极发生
E.原电池的正负极不仅与金属的活动性有关,而且也与电解质溶液有关
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com