
元素性质呈现周期性变化的基本原因是
| A.元素的原子量逐渐增大 | B.核外电子排布呈周期性变化 |
| C.核电荷数逐渐增大 | D.元素化合价呈周期性变化 |
科目:高中化学 来源: 题型:单选题
下列说法正确的是
| A.共价化合物中只含共价键,离子化合物中只含离子键 |
| B.第三周期元素形成的氢化物稳定性从左到右逐渐增强 |
| C.短周期元素形成简单离子后,最外层电子数均达到8(或2)稳定结构 |
| D.在周期表过渡元素中寻找半导体材料,在金属与非金属分界处寻找催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
元素在周围表中的位置,反映了元素的原子结构和元素的性质,下列说法正确的是
| A.同一元素不可能既表现金属性,又表现非金属性 |
| B.第三周期元素的最高正化合价等于它所处的主族序数 |
| C.短周期元素形成离子后,最外层都达到8电子稳定结构, |
| D.同一主族的元素的原子,最外层电子数相同,化学性质完全相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是( )
| A.IA族元素的金属性比IIA族元素的金属性强 |
| B.VIA族元素的氢化物中,稳定性最好的其沸点也最高 |
| C.同周期非金属氧化物对应的水化物的酸性从左到右依次增强 |
| D.第三周期元素的离子半径从左到右逐渐减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列叙述中能说明金属A肯定比金属B的活泼性强的是 ( )
| A.A原子的最外层电子数比B原子的最外层电子数少 |
| B.A原子电子层数比B原子电子层数多 |
| C.1mol A从酸中置换出的H2比1molB从酸中置换的H2多 |
| D.常温时,A能从稀盐酸中置换出氢,而B不能 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
元素周期表和元素周期律可以指导人们进行规律性的推测和判断。下列说法不合理的是
| A.若X+和Y2-的核外电子层结构相同,则原子序数:X > Y |
| B.由水溶液的酸性:HCl>H2S,可推断出元素的非金属性:Cl>S |
| C.硅、锗都位于金属与非金属的交界处,都可以做半导体材料 |
| D.Cs和Ba分别位于第六周期IA和IIA族,碱性:CsOH >Ba(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列排列顺序不正确的是
| A.热稳定性:CH4> SiH4 >HF | B.原子半径:Na>Mg>O |
| C.酸性:HClO4>H2SO4>H3PO4 | D.非金属性:F>Cl>Br |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(8分每空1分)
(1)下列3种不同粒子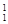 H、
H、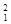 H、
H、 H表示______种元素,______种核素,
H表示______种元素,______种核素,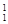 H、
H、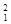 H、
H、 H互称为__________________。
H互称为__________________。
(2)下列各组物质中,互称为同分异构体的是( )
| A.水与冰 | B.O2与O3 |
C.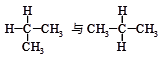 | D. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com