
下列关于丙烯(CH3﹣CH=CH2)的说法正确的( )
A. 丙烯分子有8个σ键,1个π键
B. 丙烯分子中3个碳原子都是sp3杂化
C. 丙烯分子不存在非极性键
D. 丙烯分子中3个碳原子在同一直线
考点: 共价键的形成及共价键的主要类型;极性键和非极性键;原子轨道杂化方式及杂化类型判断.
专题: 化学键与晶体结构.
分析: A.C﹣C、C﹣H键均为σ键,C=C中一个σ键,一个π键;
B.甲基中的C原子为sp3杂化,C=C中的C原子为sp2杂化;
C.同种非元素之间形成非极性键;
D.由C=C双键为平面结构、甲基为四面体结构分析.
解答: 解:A.C﹣C、C﹣H键均为σ键,C=C中一个σ键,一个π键,则丙烯分子有8个σ键,1个π键,故A正确;
B.甲基中的C原子为sp3杂化,C=C中的C原子为sp2杂化,则丙烯分子中1个碳原子是sp3杂化,2个碳原子是sp2杂化,故B错误;
C.同种非元素之间形成非极性键,则丙烯中存在C﹣C非极性共价键,故C错误;
D.由C=C双键为平面结构、甲基为四面体结构可知,丙烯分子中2个碳原子在同一直线,故D错误;
故选A.
点评: 本题考查共价键及分类,注意判断共价键的规律和常见有机物的空间结构来解答,杂化类型为解答的易错点,题目难度不大.


科目:高中化学 来源: 题型:
已知A、B、C均为短周期元素,A、B两种元素的原子具有相同数目的电子层,A元素原子最外层电子数是B元素原子最外层电子数的两倍,A元素原子M层电子数为K层电子数的3倍,C元素原子的核电荷数是电子层数的4倍,其质子数为最外层电子数的6倍.请完成下列空白:
(1)A元素为 ,C元素为 ,B元素的名称为 .
(2)A位于元素周期表中第 周期第 族
(3)C的离子结构示意图为
(4)A、B、C三种元素形成的原子半径由大到小的顺序是 (化学符号)
(5)A、B、C三种元素最高价氧化物对应的水化物中分别为 、 、 .
查看答案和解析>>
科目:高中化学 来源: 题型:
室温下,用0.100mol/L NaOH溶液分别滴定20.00ml 0.100mol/L 的盐酸和醋酸,滴定曲线如图所示,下列说法正确的是()
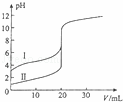
A. Ⅱ表示的是滴定醋酸的曲线
B. PH=7时,滴定醋酸消耗V(NaOH)小于20ml
C. V(NaOH)=20ml时,C(Cl﹣)=C(CH3COO﹣)
D. V(NaOH)=10ml时,醋酸溶液中:C(Na+)>C(CH3COO﹣ )>C(H+)>C(OH﹣ )
查看答案和解析>>
科目:高中化学 来源: 题型:
由CH3CH=CH2合成CH2(OOCCH3)CH(OOCCH3)CH2(OOCCH3)时,需要经过的反应( )
A. 加成→取代→取代→取代 B. 取代→加成→取代→取代
C. 取代→取代→加成→取代 D. 取代→取代→取代→加成
查看答案和解析>>
科目:高中化学 来源: 题型:
下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质);
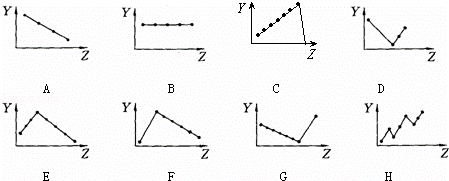
把与下面的元素有关性质相符的曲线的标号填入相应括号中:
(1)ⅡA族元素的价电子数 (2)ⅦA族元素氢化物的沸点
(3)第三周期元素单质的熔点 (4)第三周期元素的最高正化合价
(5)IA族元素单质熔点 (6)F﹣、Na+、Mg2+、Al3+四种离子的离子半径 .
查看答案和解析>>
科目:高中化学 来源: 题型:
已知Zn(s)+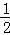 O2(g)═ZnO(s)△H=﹣350kJ/mol,则1g Zn在氧气中燃烧放出的热量约为()
O2(g)═ZnO(s)△H=﹣350kJ/mol,则1g Zn在氧气中燃烧放出的热量约为()
A. 5.4 kJ B. 350 kJ C. 3.5 kJ D. 8.5 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水.当把0.4mol液态肼和0.8mol H2O2混合反应,生成氮气和水蒸气,放出256.7kJ的热量(相当于25℃、101kPa下测得的热量).
(1)反应的热化学方程式为 .
(2)又已知H2O(l)=H2O(g)△H=+44kJ/mol.则16g液态肼与液态双氧水反应生成液态水时放出的热量是 kJ.
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)某催化剂可将汽车尾气中的CO、NO转化为无毒气体。已知:
2CO(g)+O2(g)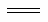 2CO2(g) ΔH=akJ·mol-1
2CO2(g) ΔH=akJ·mol-1
N2(g)+O2(g)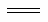 2NO(g) ΔH=b kJ·mol-1
2NO(g) ΔH=b kJ·mol-1
①反应2NO(g)+ 2CO(g)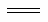 2CO2(g) +N2(g) ΔH=_________kJ·mol-1。
2CO2(g) +N2(g) ΔH=_________kJ·mol-1。
②可以利用反应:NO2+G N2+H2O+nX(n可以为零)将NO2变成无害N2,若要求X必须为无污染的物质,则G可以是_________(填写字母)。
N2+H2O+nX(n可以为零)将NO2变成无害N2,若要求X必须为无污染的物质,则G可以是_________(填写字母)。
a.NH3 b.CO2 c.SO2 d.CH3CH2OH
当反应中转移1.2mol电子时,消耗NO2__________L(标准状况)。
③用NaOH溶液吸收工业尾气中的SO2最终制得石膏(CaSO4.2H2O)。为节约资源减少排放实现物质的循环利用,生产过程中还需要加入的固体物质是____________(填化学式)。
(2)工业上通过电解含NH4F的无水熔融物生产NF3气体,其电解原理如图所示。则a极为___________极,该极的电极反应式_______________________________________。
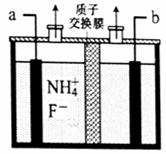
(3)用电镀法在铁板表面镀锌或锡可防腐,这种防止金属腐蚀的方法从原理上属于________________法。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com