
��������϶������������õ綯������ȼ������߽���ƶ����֡��������»����ʱ���綯���ṩ�ƶ������������͵����ģ���ɲ��������ʱ����ش��ڳ��״̬��
(1)��϶�����Ŀǰһ��ʹ�������أ��õ�������Ļ�����Ϊ�������������(��M��ʾ)Ϊ��������Һ(��ҪΪKOH)Ϊ�������Һ�������س�ŵ�ԭ��ʾ����ͼ�����ܷ�ӦʽΪ��H2��2NiOOH 2Ni(OH)2
2Ni(OH)2

����������Ϣ�жϣ���϶��������»����ʱ���ҵ缫��Χ��Һ��pH (����������������С������������)���õ缫�ĵ缫��ӦʽΪ ��
(2)Cu2O��һ�ְ뵼����ϣ���ͨ����ͼ�ĵ��װ����ȡ������ܷ�ӦΪ��2Cu��H2O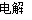 Cu2O��H2��
Cu2O��H2��

�����ĵ缫��Ӧʽ�� ��
����������Ϊ��Դ���е�⣬����������1 mol H2������ʱ��Cu2O�����۲���Ϊ g��
(3)Զ���ִ��ĸ��������ں�ˮ�������绯ѧ��ʴ�е� ��ʴ��Ϊ��ֹ���ָ�ʴ��ͨ���Ѵ�������ں�ˮ���Zn��������������Ǧ������������ֱ����Դ�� (����������������)��������
(1)����NiOOH��H2O��e��=Ni(OH)2��OH��
(2)2H����2e��=H2����144
(3)��������
��������(1)�������֪����϶��������»����ʱ�����Ӧ���ڷŵ�״̬���ʸ�����ӦʽΪ��H2��2OH����2e��=2H2O����������Ӧ�����ܵ缫��Ӧʽ��ȥ������Ӧʽ�õ�����NiOOH��H2O��e��=Ni(OH)2��OH���������ڷŵ�ʱ��������OH�������ҵ缫��Χ��Һ��pH����
(2)���װ��ͼ���ܵ�ط�Ӧʽ���Ե�֪��H���������ŵ磬��������ӦʽΪ2H����2e��=H2�������ܵ�ط�Ӧʽ����ã�1 mol H2������ʱ��ͬʱ����1 mol Cu2O��������Ϊ144 g��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014��߿���ѧ���ָ�ϰר�������1 ��ѧ����������ϰ���������棩 ���ͣ�ѡ����
NA��ʾ�����ӵ�������ֵ������˵����ȷ���ǣ�������
����ͭ���缫��ⱥ��NaCl��Һ������·��ͨ��NA������ʱ����������11.2 L���壨��״���£��������³�ѹ�£�16 g O2��16 g O3����ԭ������ΪNA������״���£�22.4 L CH3CH2OH�к��е�̼ԭ����Ϊ2NA����6.5 gпȫ������һ������Ũ���ᣬ����SO2��H2�Ļ�����壬�����������Ϊ0.1NA����10.6 g Na2CO3��ĩ�к���CO32-��Ϊ0.1NA
A���ڢܢ������������� B���٢ۢ�
C���٢ڢܢ� D���٢ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��߿���ѧһ�ָ�ϰ�κ�ѵ��ר����ϰ��һ�������棩 ���ͣ������
��֪A��B��C��D��E��F��G��H���Է�����ͼ��ʾ��ת������Ӧ�в�������������ȥ�����У�A��GΪͬһ����Ԫ�صĵ��ʣ�B��C��H��ͨ�������Ϊ���壬������C��һ���γ�����Ĵ�����Ⱦ�
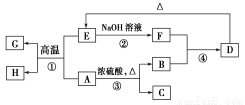
�����������գ�
��1��H��������________��
��2��E��������;��________��________��
��3����Ӧ���Ļ�ѧ����ʽ��________��
��4����Ӧ�������ӷ���ʽ��________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��߿���ѧһ�ָ�ϰ�κ�淶ѵ��9-2��ϰ���������棩 ���ͣ������
ijС��ͬѧ��������ͼװ�õ���������Һ����ȡ������������������������ء�
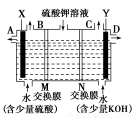
(1)X�����Դ�� (����������������)�������������� (ѡ����A������B������C������D��)�ڵ�����
(2)���ӽ���Ĥֻ����һ������ͨ������MΪ (����������������������������ͬ)����Ĥ��NΪ ����Ĥ��
(3)�����Ƶõ�����������������������Һ���Ϊ����ȼ�ϵ��(ʯīΪ�缫)�����ظ����ĵ缫��ӦʽΪ ��
(4)���ڱ�״���£��Ƶ�11.2 L����������������������� ��ת�Ƶĵ�����Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��߿���ѧһ�ָ�ϰ�κ�淶ѵ��9-2��ϰ���������棩 ���ͣ�ѡ����
��ͼ��ģ��绯ѧ��Ӧװ��ͼ������˵����ȷ���ǣ� ��
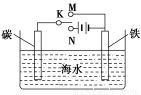
A������K����N���������缫�ĵ缫��ӦʽΪ��Fe��2e��=Fe2��
B������K����N�������Լ������ĸ�ʴ
C������K����M���������缫�ĵ缫��ӦʽΪ��2Cl����2e��=Cl2��
D������K����M�������Ӵ�̼��������K��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��߿���ѧһ�ָ�ϰ�κ�淶ѵ��9-1��ϰ���������棩 ���ͣ�ѡ����
�����ͼ�жϣ�����������ȷ���ǣ� ��
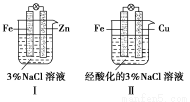
A��������������������
B���������и�����Ӧ����Fe��2e��=Fe2��
C����������������Ӧ����O2��2H2O��4e��=4OH��
D���������зֱ��������K3[Fe(CN)6]��Һ��������ɫ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��߿���ѧһ�ָ�ϰ�κ�淶ѵ��9-1��ϰ���������棩 ���ͣ�ѡ����
����ԭ��ص�������ȷ���ǣ� ��
A��ԭ��ع���ʱ���缫�ϲ�һ��������������ԭ��Ӧ
B��ij�����س䡢�ŵ�ʱ�ķ�ӦʽΪLi1��xNiO2��xLi LiNiO2���ŵ�ʱ�˵�صĸ���������Li1��xNiO2
LiNiO2���ŵ�ʱ�˵�صĸ���������Li1��xNiO2
C��Ǧ���������ṹ�ɵ�ԭ��ع���ʱ��Ǧ������5.175 gǦ�ܽ⣬�����Ͼ���1 120 mL(��״��)��������
D���������Ͽɽ���ӦCH4(g)��2O2(g)=CO2(g)��2H2O(l)����H<0��Ƴ�ԭ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��߿���ѧһ�ָ�ϰ�κ�淶ѵ��8-3��ϰ���������棩 ���ͣ������
�����£����ȡ0.1 mol��L��1 HA��Һ��0.1 mol��L��1 NaOH��Һ��������(���Ի�Ϻ���Һ����ı仯)����û����Һ��pH��8���Իش��������⣺
(1)�����Һ��pH��8��ԭ��(�����ӷ���ʽ��ʾ)�� ��
(2)�����Һ����ˮ�������c(OH��) (������������������������)0.1 mol��L��1 NaOH��Һ����ˮ�������c(OH��)��
(3)��������Һ��������ʽ�ľ�ȷ������(���������)��c(Na��)��c(A��)�� mol��L��1��c(OH��)��c(HA)�� mol��L��1��
(4)��֪NH4A��ҺΪ���ԣ���֪HA��Һ�ӵ�Na2CO3��Һ��������ų������ƶ�(NH4)2CO3��Һ��pH 7(������������������������)����ͬ�¶��µ�Ũ�ȵ���������Һ��
A��NH4HCO3 B��NH4A C��(NH4)2SO4 D��NH4Cl
��pH�ɴ�С��˳�������� (�����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��߿���ѧһ�ָ�ϰ�κ�淶ѵ��7-3��ϰ���������棩 ���ͣ������
��֪���淴Ӧ��A(g)��B(g)  C(g)��D(g)����H��0����ش��������⣺
C(g)��D(g)����H��0����ش��������⣺
(1)��ij�¶��£���Ӧ�����ʼŨ�ȷֱ�Ϊ��c(A)��1 mol/L��c(B)��2.4 mol/L���ﵽƽ��ʱ��A��ת����Ϊ60%����ʱB��ת����Ϊ ��
(2)����Ӧ�¶Ƚ��ͣ���B��ת���ʽ� (����������������С������������)��
(3)����Ӧ�¶Ȳ��䣬��Ӧ�����ʼŨ�ȷֱ�Ϊc(A)��4 mol��L��1��c(B)��a mol��L��1���ﵽƽ���c(C)��2 mol��L��1����a�� ��
(4)����Ӧ�¶Ȳ��䣬��Ӧ�����ʼŨ�ȷֱ�Ϊc(A)��c(B)��b mol/L���ﵽƽ���c(D)�� ��(������λ��Ч����)
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com