
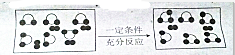
 假设一定条件下某密闭容器中存在如图所示反应(空心球代表X原子,实心球代表Y原子),下列有关该反应的说法中不正确的是( )
假设一定条件下某密闭容器中存在如图所示反应(空心球代表X原子,实心球代表Y原子),下列有关该反应的说法中不正确的是( )| A、该反应一定是可逆反应 |
| B、该反应一定是氧化还原反应 |
| C、该反应一定是放热反应 |
| D、该反应的方程式可表示为2XY2+Y2?2XY3 |
 和2个
和2个 反应生成4个
反应生成4个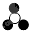 ,该反应的方程式可表示为2XY2+Y2?2XY3,故D正确;
,该反应的方程式可表示为2XY2+Y2?2XY3,故D正确;

 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案科目:高中化学 来源: 题型:
| A、0.1mol Fe与0.1mol Cl2充分反应,转移的电子数为0.3NA |
| B、1mol H2O2完全分解生成H2O和O2时,转移了NA个电子 |
| C、1mol C10H22分子中,含有共价键数目为32NA |
| D、0.5mol Na2O2中含有NA个阴离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
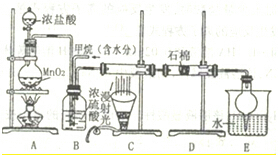
| V(Cl2) |
| V(CH4) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 浓H2SO4 |
| △ |
| Br2 |
| CCl4 |
| A、CH3CH2CHBrCH2Br |
| B、CH3CH(CH2Br)2 |
| C、CH3CHBrCHBrCH3 |
| D、(CH3)2CBrCH2Br |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CaO--干燥剂 |
| B、Na2O2--供氧剂 |
| C、Al2O3--铝热剂 |
| D、KAl(SO4)2.12H2O--净水剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
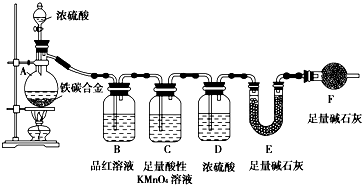 现有铁、碳两种元素组成的合金,某实验小组为了研究该合金的性质并测定该合金中碳的质量分数,设计了如下实验方案和实验装置:
现有铁、碳两种元素组成的合金,某实验小组为了研究该合金的性质并测定该合金中碳的质量分数,设计了如下实验方案和实验装置:| 滴加的溶液 | 氯水 | 氨水 |
| 沉淀的化学式 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH3CH2CH2COOCH2CH(CH3)2 |
| B、CH3 COOCH(CH3)2 |
| C、CH3 COOCH2CH2CH2OOCCH3 |
| D、CH3 COOCH2CH3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com