
设NA为阿伏加德罗常数的值。下列说法正确是
A.标准状况下,2.24 L三氯甲烷中含有碳氯共价健的数目为0.3NA
B.25℃时,1 L pH=12的Na2CO3溶液中含有Na+的数目为0.02NA
C.常温常压下,28 g C2H4、C3H6的混合气体中含有碳原子的数目为2NA
D.0.1 mol Cl2全部溶于水后转移电子的数目为0.1NA
科目:高中化学 来源:2014-2015学年山东省高三上学期期中考试化学试卷(解析版) 题型:选择题
X、Y、Z、M四种金属,已知X可以从Y的盐溶液中置换出Y:X和Z作原电池电极时,Z为正极;Y和Z的离子共存于电解液中,Y离子先放电;M的离子的氧化性强于Y的离子。则这四种金属的活动性由强到弱的顺序为
A.X>Y>Z>M B.X>Z>M>Y C.M>Z>X>Y D.X>Z>Y>M
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省盐城市高三第二次调研考试化学试卷(解析版) 题型:选择题
某碱性溶液中只含有Na+、CH3COO-、H+、OH-四种离子。下列描述正确的是
A.该溶液可能由等物质的量浓度、等体积的NaOH溶液和CH3COOH溶液混合而成
B.该溶液一定由pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合而成
C.该溶液中离子浓度一定为c (Na+)>c(CH3COO-)>c (OH-)>c(H+)
D.加入一定量冰醋酸,c(CH3COO-)可能大于、等于或小于c(Na+)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省无锡市高三期中化学试卷(解析版) 题型:填空题
(12分)酸浸法制取硫酸铜的流程示意图如下
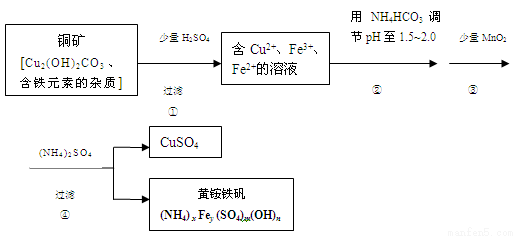
(1)步骤①中Cu2(OH)2CO3 发生反应的化学方程式为 。
(2)在步骤③发生的反应中,1mol MnO2转移2mol 电子,该反应的离子方程式为 。
(3)该小组为测定黄铵铁矾的组成,进行了如下实验:
a.称取4.800 g样品,加盐酸完全溶解后,配成100.00 mL溶液A;
b.量取25.00 mL溶液A,加入足量的KI,用0.2500 mol·L-1Na2S2O3溶液进行滴定(反应方程式为I2+2Na2S2O3=2NaI+Na2S4O6),消耗30.00 mLNa2S2O3溶液至终点。
b.量取25.00 mL溶液A,加入足量的NaOH溶液充分反应后,过滤、洗涤、灼烧得红色粉末0.600g。
c.另取25.00 mL溶液A,加足量BaCl2溶液充分反应后,过滤、洗涤、干燥得沉淀1.165 g。
①用Na2S2O3溶液进行滴定时,滴定到终点的颜色变化为 。
②通过计算确定黄铵铁矾的化学式(写出计算过程)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省无锡市高三期中化学试卷(解析版) 题型:选择题
下列有关说法正确的是
A.镀铜铁制品镀层受损后,铁制品比受损前更容易生锈
B.反应Hg(l)+H2SO4(aq)===HgSO4(aq)+H2(g)在常温下不能自发进行,则ΔH<0
C.N2(g)+3H2(g) 2NH3(g) △H<0,其他条件不变时升高温度,反应速率v(H2)和氢气的平衡转化率均增大
2NH3(g) △H<0,其他条件不变时升高温度,反应速率v(H2)和氢气的平衡转化率均增大
D.CH3COOH溶液加水稀释后,溶液中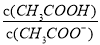 的值减小
的值减小
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省无锡市高三期中化学试卷(解析版) 题型:选择题
2014年的南京青奥会将秉持“绿色青奥”这一理念,下列行为不符合这一主题的
A.推广使用一次性木筷,减少疾病传染
B.推广使用电动汽车、天然气汽车等环保公共交通工具
C.大力发展太阳能和风力发电机可缓解电力紧张问题
D.将地沟油回收加工为燃料油,提高资源的利用率
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省宿迁市高三上学期第一次摸底考试化学试卷(解析版) 题型:选择题
氮氧化物与悬浮在大气中海盐粒子的相互反应:
4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+ Cl2(g),ΔH
2NaNO3(s)+2NO(g)+ Cl2(g),ΔH
在恒温条件下,向2 L恒容密闭容器中加入0.4mol NO2和0.2 mol NaCl,10 min反应达到平衡时n(NaNO3)=0.1mol,NO2的转化率为α。下列叙述中正确的是
A.10min内NO浓度变化表示的速率v(NO)=0.01 mol·L-1·min-1
B.若保持其他条件不变,在恒压下进行该反应,则平衡时NO2的转化率大于α
C.若升高温度,平衡逆向移动,则该反应的ΔH>0
D.若起始时向容器中充入NO2(g) 0.1 mol、NO(g)0.2 mol和Cl2(g)0.1 mol(固体物质足量),则反应将向逆反应方向进行
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省连云港市高三上学期期中化学试卷(解析版) 题型:实验题
(16分)海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如下:

(1)指出提取碘的过程中有关的实验操作名称:① ,② 。
(2)氧化时,在三颈烧瓶中将含I-的水溶液用盐酸调至pH约为2,缓慢通入Cl2,在40℃左右反应(实验装置如图所示)。

实验控制在较低温度下进行的原因是 ;锥形瓶里发生反应的离子方程式为
(3)在第②步操作过程中,可加入的有关试剂是 。
A.酒精 B.四氯化碳 C.醋酸 D.苯
(4)含碘离子的溶液也可以采用下图方法得到碘
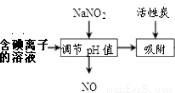
①加入NaNO2并调节pH<4,反应的离子方程式 __________________。
②流程中生成的NO尾气有毒,工业上将其与O2按一定比例通入NaOH制备NaNO2,
写出反应的化学方程式: ____________________。
(5)要测量含碘离子的溶液中I-的浓度,取25 mL该溶液,先加几滴KSCN溶液,再逐滴滴入0.1 mol·L-1FeCl3溶液, 若消耗FeCl3溶液20.4 mL,则含碘离子的溶液中I-的浓度为 。(保留两位有效数字)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年重庆复旦中学高一上学期期中化学试卷(解析版) 题型:选择题
在标准状况下,下列气体含有的分子数最多的是
A.36.5g HCl B.22.4L O2 C.4g H2 D.0.5mol SO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com