
| 3 |
| 4 |
 ;
; ;
;
|


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

 ,所以它属于二肽
,所以它属于二肽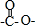 结构且能发生银镜反应 ②N原子直接与苯环相连③核磁共振氢谱有5种峰且峰面积比1:1:2:2:3,
结构且能发生银镜反应 ②N原子直接与苯环相连③核磁共振氢谱有5种峰且峰面积比1:1:2:2:3,查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 滴定前 | 第一次 终点 | 第二次 终点 | 第三次 终点 | |
| 碱式滴定管 液面刻度 | 0.10mL | 19.12mL | 18.15mL | 19.08mL |

查看答案和解析>>
科目:高中化学 来源: 题型:
| C |
| D |
查看答案和解析>>
科目:高中化学 来源: 题型:
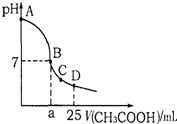 在25mL0.1mol?L-1NaOH溶液中逐滴加入0.2mol?L-1CH3COOH溶液,溶液pH变化曲线 如图所示,下列有关离子浓度的关系正确的是( )
在25mL0.1mol?L-1NaOH溶液中逐滴加入0.2mol?L-1CH3COOH溶液,溶液pH变化曲线 如图所示,下列有关离子浓度的关系正确的是( )| A、在A、B间,溶液中可能有c(Na+)>c(OH-)>c(CH3COO-)>c(H+) |
| B、在B点,a>12.5,且有c(Na+)=c(CH3COO-)=c(OH-)=c(H+) |
| C、在C点,c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
| D、在D点,c(CH3COO-)+c(CH3COOH)=c(Na+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com