
【题目】我国科学家成功实现甲烷在催化剂及无氧条件下,一步高效生产乙烯、芳香烃和氢气等化产品,为天然气化工开发了一条革命性技术。以甲烷为原料合成部分化工产品流程如图(部分反应条件已略去):

(1)E中官能团的名称为___,C物质的结构简式为___。
(2)上述③~⑥转化反应中,属于取代反应的有___(用反应序号填写)。
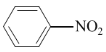
(3)写出反应⑦的反应方程式:__。
(4)实验室制备物质E时,装置如图所示(加热和夹持装置已省略)。试管a中实验前盛放的物质是___,实验后出现分层现象,分离物质D需要的玻璃仪器有___和烧杯等。

(5)某同学在试管b中加入6.0克乙酸和足量乙醇采用适当条件使反应充分进行,结束后在试管b回收到3.0克乙酸,则该同学在本次实验中制得乙酸乙酯的最大质量为___。
【答案】酯基 CH3CHO ⑥ ![]() +HO-NO2
+HO-NO2![]()
 +H2O 饱和碳酸钠溶液 分液漏斗 4.4g
+H2O 饱和碳酸钠溶液 分液漏斗 4.4g
【解析】
根据流程,B→C→D是连续被氧化的过程,B为醇,C为醛,D为酸,B与D发生酯化反应得到E,即E为酯,从而推出B为CH3CH2OH,C为CH3CHO,D为CH3COOH,E为CH3COOCH2CH3,A与H2O发生加成反应得到B,即A为CH2=CH2,据此分析;
(1)根据上述分析,E为乙酸乙酯,含有的官能团是酯基;C的结构简式CH3CHO;
(2)根据上述分析,③为加成反应,④为氧化反应,⑤为氧化反应,⑥为取代反应,即属于取代反应的是⑥;
(3)反应⑦发生硝化反应,即反应方程式为![]() +HO-NO2
+HO-NO2![]()
 +H2O;
+H2O;
(4)实验室制备乙酸乙酯,试管a中试剂为饱和碳酸钠溶液,能溶解乙酸、吸收乙酸、降低乙酸乙酯的溶解度便于分离提纯;需要通过分液获得乙酸乙酯,需要玻璃仪器是分液漏斗和烧杯;
(5)加入6.0g乙酸和过量的乙醇,反应结束后回收到3.0g乙酸,说明有3.0g乙酸参与反应,令生成乙酸乙酯的质量为mg,则有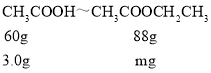 ,解得m=4.4g。
,解得m=4.4g。


科目:高中化学 来源: 题型:
【题目】我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程。该历程示意图如下。

下列说法不正确的是
A. 生成CH3COOH总反应的原子利用率为100%
B. CH4→CH3COOH过程中,有C―H键发生断裂
C. ①→②放出能量并形成了C―C键
D. 该催化剂可有效提高反应物的平衡转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W的原子序数依次增大,它们原子的最外层电子数之和为14。Z是短周期主族元素中原子半径最大的元素,Z与X原子的最外层电子数相同,Y与W同主族。下列说法正确的是( )
A.X与Y只能形成一种化合物
B.原子半径:r(Y)<r(W)<r(Z)
C.W的简单气态氢化物的热稳定性比Y的强
D.Z的最高价氧化物对应的水化物是酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“神十”宇航员使用的氧气瓶是以聚酯玻璃钢为原料。甲、乙、丙三种物质是合成聚酯玻璃钢的基本原料。下列说法不正确的是( )
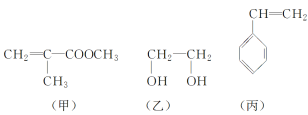
A.甲物质在一定条件下可以生成有机高分子化合物
B.1mol乙物质可与2mol钠完全反应生成2mol氢气
C.甲、乙、丙物质都能够使溴的四氯化碳溶液褪色
D.丙可以使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数。下列说法正确的是( )
A. 1mol月球背面的氦—3(3He)含有质子为2NA
B. 标况下,22.4L甲烷和1molCl2反应后的混合物中含有氯原子数小于2NA
C. 2molSO2与1molO2充分反应,转移的电子数为4NA
D. 25℃时,1L pH=13的Ba(OH)2溶液中含有OH-的数目为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,回答下列问题:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
1 | ① | |||||||
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ |
(1)③、④、⑤的原子半径由大到小的顺序为___(用元素符号回答)。
(2)②、③、⑦的最高价氧化物对应的水化物酸性由强到弱的顺序是___。(用化学式回答)
(3)②、⑧两种元素形成的某化合物是一种常见的有机溶剂,写出该化合物的电子式___。
(5)⑦的最简单氢化物是一种无色气体,遇到空气能发生爆炸性自燃。已知室温下1g该氢化物自燃放出45.0kJ的热量(产物为⑦的氧化物和液态水),其热化学方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2广泛用于医药、硫酸工业等领域,回收废气中的SO2可用如下方法。
方法Ⅰ | 用碱式硫酸铝Al2(SO4)x(OH)y溶液吸收富集SO2 |
方法Ⅱ | 在Fe2+或Fe3+催化下,用空气(O2)将SO2氧化为H2SO4 |
(1)方法Ⅰ的过程如下。
① 制备Al2(SO4)x(OH)y。向Al2(SO4)3溶液中加入CaO粉末,调pH至3.6。 CaO的作用是______
② 吸收:Al2(SO4)x(OH)y吸收SO2后的产物是______(写化学式)。
③ 解吸:加热②中产物,产生SO2,Al2(SO4)x(OH)y再生。
(2)方法Ⅱ中,在Fe2+催化下,SO2、O2和H2O生成H2SO4的化学方程式是______。
(3)方法Ⅱ中,Fe2+的催化过程可表示如下:
ⅰ:2Fe2++O2+SO2=2Fe3++SO42-
ⅱ:……
① 写出ⅱ的离子方程式:______。
② 下列实验方案可证实上述催化过程。将实验方案补充完整。
a.向FeCl2溶液滴入KSCN,无变化
b.向FeCl2溶液通入少量SO2,滴入KSCN,颜色变红。
c.取b中溶液,______。
(4)方法Ⅱ中,催化氧化后,采用滴定法测定废气中残留SO2的含量。将V L(已换算为标准状况)废气中的SO2用1%的H2O2完全吸收,吸收液用如图所示装置滴定,共消耗a mL c mol/L NaOH标准液。

①H2O2氧化SO2的化学方程式______。
② 废气中残留SO2的体积分数为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示。若Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是( )

A.原子半径:W>Z>Y>X
B.最高价氧化物对应水化物的酸性:Z>W>X
C.四种元素的单质中,Z单质的熔、沸点最低
D.W的单质能与水反应,生成一种具有漂白性的物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁稀土合金广泛应用于航空、航天、电子、通讯和汽车制造业等领域。熔盐电解法是一种高效制备镁稀土合金的方法,实验室制取Mg-Gd合金(物质的量比为1:1)的电解槽示意图如下(相对原子质量Mg—24,Gd—157),下列说法正确的是

A.添加LiF、BaF2的作用是催化剂
B.阳极的电极反应式为2F——2e—= F2 ↑
C.当电路中通过0.1mol电子时,生成Mg- Gd合金的质量为3.62 g
D.电解结束后,铝、碳电极质量不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com