
����Ŀ��������������Ⱦ�ϵ���Ҫԭ�ϡ�ijͬѧ��ʵ����������ͼװ����ȡ����������Ҫ�������£�

���ڴ��Թ��ォ2mLŨ�����1.5mLŨ�����ϣ�ҡ�ȣ���ȴ��50��60�����¡�Ȼ����μ���1mL�����ߵα����Թܡ�
�ڰ�ͼ���Ӻ�װ�ã������Թܷ���60���ˮԡ�м���10���ӡ�
���������գ�
��1��ָ��ͼ�еĴ���_________________��________________��
��2���������м��뱽ʱ������μ��롱�����ߵα����Թܡ���Ŀ����________________����Ӧһ��ʱ����Һ���Է�Ϊ���㣬�ϲ��___________ɫ��������Ҫ������_____________����д�������ƣ����ѷ�Ӧ��Ļ��Һ����ʢ����ˮ���ձ�����裬���Կ���_____����ѡ���ţ�
a.ˮ�����Ǻ������ʵ������� b.ˮ����dz��ɫ��������ζ��Һ��
c.�ձ��е�Һ̬�л���ֻ�������� d.����ɫ����״Һ�帡��ˮ��
��3��Ϊ�˻�ô���������ʵ�鲽��Ϊ����ˮϴ�����룻�ڽ���������ת�Ƶ�ʢ��_____________���ձ���ϴ�ӡ���______________����д�������ƣ����з��룻��_____________���ܸ����____________��
��4��ʵ��װ�þ��Ľ���ͬѧ��������ʵ�鲽�����½����˶��ʵ��,��ַ�Ӧ��������������֣������������
��1�����ʵ�������ֵ��ԭ����_____________________________________________��
��2�����ʸ�������ֵ��ԭ����___________________________________________��
���𰸡� ȱ���¶ȼ� ���ԹܽӴ��ձ��ײ�������������˵���� ʹ��������Ͼ��ȡ��ܼ�ʱ���߷�Ӧ�����������������������𰸣� dz��ɫ ���������� b��d ����������Һ ��Һ©�� ˮϴ�������ˮϴ ���� �¶ȹ�����������ķֽ⡢���Ļӷ� �¶ȹ��ߣ��������������������IJ������ɣ����и���Ӧ��������������Ⱥ�����
����������1����ˮԡװ����Ϊ�˾�ȷ����ʵ���¶ȣ���Ҫ���¶ȼƲ���ˮԡ���¶ȣ�Ϊʹ���Ⱦ��ȣ��Թܲ��ܽӴ����ձ��ײ���
��2������������Ӧ��һ�����ȷ�Ӧ���������������м��뱽ʱҪ��μ��룬�ߵα����Թܣ��Է�ֹ�Թ���Һ�����Թܣ�������뱽��Ӧһ��ʱ��������������Լ�����δ��Ӧ�ı����ḡ�ڻ������ϲ㣬�ѷ�Ӧ��Ļ��Һ����ʢ����ˮ���ձ����Ӧ��δ��Ӧ�ı��ḡ��ˮ�ϲ㣬���������ˮ�����ɵ���������ˮ����·���
��3�����ᴿ�������Ĺ����У������������ᣬ����Ӧ�����������б��������������ܣ����ݷ������ֲ����ܺͻ��ܵ�Һ��ķ������в�����
��4���ڱ�ʵ�������ʵ���¶ȹ��ᵼ������ķֽ⡢���Ļӷ�����ʹ���ʽ��ͣ�Ҳ��ʹ���������л���ӷ������ɵ��������У�ʹ������������ʹ��ʵ��ֵ��������ֵ��
��1����ˮԡװ����Ϊ�˾�ȷ����ʵ���¶ȣ���Ҫ���¶ȼƲ���ˮԡ���¶ȣ�Ϊʹ���Ⱦ��ȣ��Թܲ��ܽӴ����ձ��ײ���������ͼ�д���Ϊȱ���¶ȼơ����ԹܽӴ��ձ��ײ���
��2������������Ӧ��һ�����ȷ�Ӧ���������������м��뱽ʱҪ��μ��룬�ߵα����Թܣ�ʹ��������Ͼ��ȣ�����ܼ�ʱ���߷�Ӧ��������������ֹ�Թ���Һ�����Թܣ�������뱽��Ӧһ��ʱ��������������Լ�����δ��Ӧ�ı����ḡ�ڻ������ϲ㣬�ѷ�Ӧ��Ļ��Һ����ʢ����ˮ���ձ����Ӧ��δ��Ӧ�ı��ḡ��ˮ�ϲ㣬���������ˮ�����ɵ���������ˮ����·��������ϲ��dz��ɫ��������Ҫ�������������������ѷ�Ӧ��Ļ��Һ����ʢ����ˮ���ձ�����裬���Կ���ˮ����dz��ɫ��������ζ��Һ�壬ͬʱ����ɫ����״Һ�帡��ˮ�棬��ѡb��d��
��3�����ᴿ�������Ĺ����У������������ᣬ����Ӧ�����������б��������������ܣ����Բ�������Ϊ����ˮϴ�����룻�ڽ���������ת�Ƶ�ʢ������������Һ���ձ���ϴ�ӡ��÷�Һ©�����з��룻��ˮϴ�����룻�ܸ��������
��4���ڱ�ʵ�������ʵ���¶ȹ��ᵼ������ķֽ⡢���Ļӷ�����ʹ���ʽ��ͣ�Ҳ��ʹ���������л���ӷ������ɵ��������У�ʹ������������ʹ��ʵ��ֵ��������ֵ��


 ���ʿ��ÿ��ֳɳ�ϵ�д�
���ʿ��ÿ��ֳɳ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��75��Ԫ��画��۵�������٣������캽�շ������ı���Ԫ�ء��ؿ���蝹ĺ������ͣ���������⡢ͭ��п��Ǧ�ȿ����С��ش���������:
��1������華���ͬһ�壬��ԭ�Ӽ۲���ӵĹ����ʾʽ(�۲�����Ų�ͼ)Ϊ_______�����������ڱ���_____����
��2����練�����ͭ���γɶ���������:���������ͭ(I)[Cu(NH3)2]Ac���������պϳɰ��жԴ����к���CO���壺[Cu(NH3)2Ac+CO+NH3![]() [Cu(NH3)3]Ac��CO��(Ac��ʾ�����)
[Cu(NH3)3]Ac��CO��(Ac��ʾ�����)
����ͭ�����γ������ķ��ӻ�����Ӧ�߱��Ľṹ������___________________________��
����λ��NH3��Nԭ�ӵ��ӻ�����Ϊ_____��1mol ������[Cu(NH3)2]+�к�����������ĿΪ______��
��д����CO ��Ϊ�ȵ������һ�����ӵĻ�ѧʽ__________________��
��3������蝹��۵�����̣��Դ�ԭ�ӽṹ�ĽǶȼ��Խ���_________________________________________________��
��4���������Ϊ������������������Ϊ3.74A(1A=10-10m)���ԭ��ռ�ݶ��㣬��ԭ��ռ���������ġ����ԭ�ӵ���λ��Ϊ_______��������蝹��ܶ�Ϊ____g/cm3��(��NA��ʾ�����ӵ�������ֵ��д����ʽ����)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ֧25 mL����ʽ�ζ�����ʢ��0.lmol��L��1HCl��Һ����Һ��ǡ����5 mL�Ŀ̶ȴ������ѵζ����е���Һȫ�������ձ��У�Ȼ����0.lmol��L��1 NaOH ��Һ�����кͣ������� NaOH ��Һ�����
A. ����20 mL B. ��20 mL C. ����20 mL D. ����5 mL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʵ���Һ�У�������������������(����)
A. Na2S B. Na3PO4 C. Na2CO3 D. AlCl3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����״̬�£���̬���ӶϿ�1 mol��ѧ�����ʱ��Ϊ���ܣ���֪H��H��H��O��O�TO���ļ��ܡ�H�ֱ�Ϊ436kJ/mol��463kJ/mol��495kJ/mol�������Ȼ�ѧ����ʽ��ȷ���ǣ�������
A.H2O ��g���TH2��g��+ ![]() O2��g������H�T��485 kJ/mol
O2��g������H�T��485 kJ/mol
B.2H2��g��+O2��g���T2H2O��g������H�T��485 kJ/mol
C.2H2��g��+O2 ��g���T2H2O��g������H�T+485 kJ/mol
D.H2O ��g���TH2��g��+ ![]() O2��g������H�T+485 kJ/mol
O2��g������H�T+485 kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�������ʹ�÷�����ʵ�������ȷ���ǣ� ��
A. ������ƿ������Һʱ������ˮ�����̶��ߣ������õζ�����������Һ��
B. ��ʽ�ζ���װ��Һǰ���������ø���Һ��ϴ
C. ����к͵ζ�ʵ���У��ô�����Һ��ϴ��ƿ�Լ�Сʵ�����
D. ϴ������ƿ������ƿ���ԷŽ������к��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ȼ�������������е����⣬��������ȡ���������յ������ɼ��ٶԻ�������Ⱦ��
�ش��������⣺
��1����һ���������£���Ȼ���������лᷢ�����·�Ӧ��
2H2S(g)+3O2(g)=2SO2(g)+2H2O(g) ��H1
4H2S(g)+SO2(g)=3S2(g)+4H2O(g) ��H2
2H2S(g)��O2(g)=2S(g)+2H2O(g) ��H3
����ͬ�����·�Ӧ2S(g)=S2(g)����H=_______���ú���H1����H2����H3�Ĵ���ʽ��ʾ����
��2������ֽⷴӦ2H2S(g)![]() 2H2(g)+S2(g)����101 kPaʱ�����������������¶ȵĹ�ϵ����ͼ��ʾ��
2H2(g)+S2(g)����101 kPaʱ�����������������¶ȵĹ�ϵ����ͼ��ʾ��

���÷�Ӧ����H______0�������������������
��Ϊ���H2S��ƽ��ֽ��ʣ����ı��¶��⣬���ɲ�ȡ�Ĵ�ʩ��______________________________��
��ͼ��A��ʱ��Ӧ��ƽ�ⳣ��Kp=______����ƽ���ѹ����Ũ�ȣ�ƽ���ѹ=��ѹ�����ʵ�����������
��3���ҹ�ѧ�߷�����һ�ַֽ��������Ⲣ�������װ������ͼ��ʾ��

����װ��������ת���ķ�ʽΪ____________________________________________________��
����Y��Һ�еĵ��(A/B)ѡ��I3-/I-��װ�ù���ʱY���ϵĵ缫��ӦʽΪ__________________________��Y����Һ�з��������ӷ�ӦΪ________________________________�����о�һ�ֿ���ΪY��ѭ��Һ�����ĵ�ԣ�_______________��
���÷ֽ�H2S����ķ�����Ҫ�ŵ���_____________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����չ��ѧ��ѧʵ���о��������塣ͨ���о������Է���һЩʵ��װ�õIJ��㣬�Ӷ����ڴ˻����ϸĽ�ʵ�֡�
��1��ͼ��Ϊij�汾�̲���ͭ��Ũ���ᷴӦ��ʵ��װ�á�

��ͭ��Ũ���ᷴӦ�Ļ�ѧ����ʽ��________________________��
��װ��������������Һ��������___________________________��
��2��С���Ը�ʵ�������ͼ�ҵĸĽ���װ���Һͼ���ȣ�ʵ������о��е��ŵ���___________��
��3����ͼ����ʾװ�ý���ʵ��ʱ��С���������³鶯ͭ˿ʱ�������Թ�����������������ľ���ݳ�����������ͼ���ĸĽ���
��������ͼװ���ռ�һ�Թ�NO2�����ڷ����ڻ�����Ӧ��װ��ͼ________��
��������ͼװ�ý���ʵ�飬ʵ����Ҳ�����ҵ��ŵ㡣Ҫʵ����һ�ŵ㣬ʵ�������Ӧ���еIJ�����____________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ���õ�ⷨ�����������������ζ�ˮ�����Ⱦ��ģ�����ͼ��ʾ,����˵������ȷ����
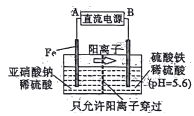
A. A��B�ֱ�Ϊֱ����Դ����������
B. �о����������Ҳ�����pH��Сʱ�����������ݳ�,������˵��H+��������ǿ������c(H+)�й�
C. �������У�����������η�����ӦΪ:Fe-2e-=Fe2+ 2NO2-+8H++6Fe2+=N2��+6Fe3++4H2O
D. ��������ת��0.6mol����ʱ,���������������1.4g
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com