
【题目】某些化学问题可用相似的示意图来表示。下列说法不正确的是![]()
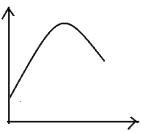
选项 | 横坐标 | 纵坐标 | 研究对象 |
A | 反应时间 | 溶液温度 | 足量镁条放在 |
B | 反应温度 | 反应速率 | 酶催化反应 |
C | 盐酸体积 | 沉淀质量 |
|
D | 反应过程 | 能量 |
|
A.AB.BC.CD.D
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列说法不正确的是:
A. 在一个氧化还原反应中,氧化剂的氧化性强于氧化产物
B. 在一个氧化还原反应中,还原产物的还原性弱于还原剂
C. amolH2SO4中,含有b个氧原子,则阿伏加德罗常数可以表示为b/4a/mol
D. 配制0.05mol/LNa2CO3溶液90mL,需Na2CO3固体5.3g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下说法中正确的是( )
①仅用试管、胶头滴管、溴水、KI淀粉溶液就可比较Br2与I2的氧化性的强弱
②利用烧杯、玻璃棒、胶头滴管、分液漏斗及溴水和CCl4能除去NaBr溶液中的少量NaI
③海水提溴与海带提碘均涉及氧化还原反应
④制备粗硅的反应为C+SiO2![]() Si+CO2↑
Si+CO2↑
⑤SiO2与Al2O3均能与强碱溶液反应,所以均为酸性氧化物
⑥光导纤维的成分主要是Si
A.①②③B.②③④
C.②④⑥D.①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在25 ℃条件下向10.00 mL 0.1 mol·L-1HCOOH溶液中逐滴加入0.1 mol·L-1NaOH溶液,其pH变化曲线如下图所示(忽略温度变化)。下列说法中不正确的是( )
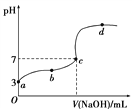
A. a点表示的溶液中c(HCOO-)约为10-3 mol·L-1
B. 用25 mL的酸式滴定管量取HCOOH溶液
C. c点NaOH溶液的体积小于10 mL
D. 在a、c间任一点,溶液中一定都有c(Na+)>c(HCOO-)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向![]() 溶液中,不断通入HCl气体
溶液中,不断通入HCl气体![]() 忽略溶液体积变化
忽略溶液体积变化![]() ,得到
,得到![]() 和
和![]() 与pH的变化关系如图所示,则下列说法不正确的是
与pH的变化关系如图所示,则下列说法不正确的是![]()
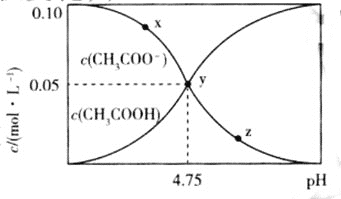
A.溶液中水的电离程度:![]()
B.在y点时,通入的HCl气体在标准状况下的体积为![]()
C.随着HCl的通入,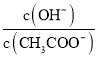 不断减小
不断减小
D.该温度下,![]() 的
的![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温时,![]() 的
的![]() 和
和![]() 的
的![]() 两种碱溶液,起始时的体积均为
两种碱溶液,起始时的体积均为![]() ,分别向两溶液中加水进行稀释,所得曲线如图所示
,分别向两溶液中加水进行稀释,所得曲线如图所示![]() 表示溶液的体积
表示溶液的体积![]() ,
,![]() 。下列说法不正确的是
。下列说法不正确的是![]()
![]()
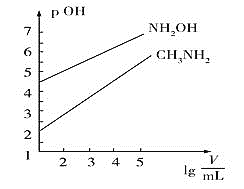
A.![]() 的电离常数
的电离常数![]() 的数量级为
的数量级为![]()
B.用相同浓度的盐酸分别滴定上述两种碱溶液至![]() ,消耗盐酸体积:
,消耗盐酸体积:![]()
C.当两溶液均稀释至![]() 时,溶液中水的电离程度:
时,溶液中水的电离程度:![]()
D.浓度相同的![]() 和
和![]() 的混合溶液中离子浓度大小关系:
的混合溶液中离子浓度大小关系:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,![]() 的
的![]() 溶液中,
溶液中,![]() 、
、![]() 、
、![]() 三者所占物质的量分数
三者所占物质的量分数![]() 分布系数
分布系数![]() 随pH变化的关系如图所示。下列表述不正确的是
随pH变化的关系如图所示。下列表述不正确的是
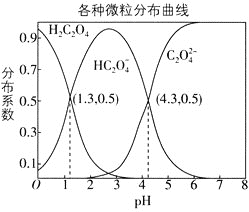
A.![]() 的平衡常数
的平衡常数![]()
B.将等物质的量的![]() 、
、![]() 溶于水中,所得溶液pH恰好为
溶于水中,所得溶液pH恰好为![]()
C.常温下HF的电离常数![]() ,将少量
,将少量![]() 溶液加入到足量NaF溶液中,发生的反应为:H2C2O4+F-=HF+HC2O4-
溶液加入到足量NaF溶液中,发生的反应为:H2C2O4+F-=HF+HC2O4-
D.在![]() 溶液中,各离子浓度大小关系为
溶液中,各离子浓度大小关系为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是一种优良的水处理剂。25℃,其水溶液中加酸或碱改变溶液的pH时,含铁粒子的物质的量分数δ(X)随pH的变化如图所示[已知δ(X)=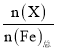 ]。下列说法正确的是( )
]。下列说法正确的是( )

A.K2FeO4、H2FeO4都属于强电解质
B.25℃,H2FeO4+H+![]() H3FeO4+的平衡常数K>100
H3FeO4+的平衡常数K>100
C.由B点数据可知,H2FeO4的第一步电离常数Ka1=4.15×10-4
D.A、C两点对应溶液中水的电离程度相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化工厂制备净水剂硫酸铁铵晶体![]() 的一种方案如下:
的一种方案如下:

下列说法不正确的是![]()
A.滤渣A的主要成分是![]()
B.“合成”反应要控制温,温度过高,产率会降低
C.“系列操作”包括蒸发浓缩、冷却结晶、过滤、洗涤、干燥等
D.相同条件下,![]() 净水能力比
净水能力比![]() 强
强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com