
【题目】下列关于盐类水解的应用的说法正确的是( )
A.加热蒸干Na2CO3溶液,最后可以得到NaOH和Na2CO3的混合固体
B.除去MgCl2溶液中的Fe3+,可以加入NaOH固体
C.明矾净水过程中发生的反应:Al3++3H2O![]() Al(OH)3(胶体)+3H+
Al(OH)3(胶体)+3H+
D.加热蒸干KCl溶液,最后得到KOH固体(不考虑CO2的反应)
【答案】C
【解析】
A.Na2CO3在溶液中水解生成碳酸氢钠和氢氧化钠,水解方程式为:Na2CO3+H2ONaOH+NaHCO3,由于生成的NaOH不挥发,氢氧化钠能够与碳酸氢钠发生中和反应生成碳酸钠和水,所以将Na2CO3溶液加热蒸发后最终得到的固体仍然为Na2CO3,A错误;
B.Mg2+、Fe3+都能与NaOH反应,所以加NaOH不能除去MgCl2中的Fe3+,B错误;
C.明矾在水中电离出Al3+,Al3+水解生成的Al(OH)3胶体具有吸附性,即Al3++3H2OAl(OH)3(胶体)+3H+,C正确;
D.KCl在溶液中不水解,加热蒸干KCl溶液,最后得到KCl固体,D错误;
故合理选项是C。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】已知:①2H2(g)+O2(g)=2H2O(l) ΔH1=-571.6 kJ·mol-1
②2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH2=-1452 kJ·mol-1
③H+(aq)+OH-(aq)=H2O(l) ΔH3=-57.3 kJ·mol-1
下列说法正确的是( )
A. H2(g)的燃烧热为571.6 kJ·mol-1
B. 同质量的H2(g)和CH3OH(l)完全燃烧,H2(g)放出的热量多
C. ![]() H2SO4(aq)+
H2SO4(aq)+![]() Ba(OH)2(aq)=
Ba(OH)2(aq)=![]() BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1
BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1
D. 3H2(g)+CO2(g)=CH3OH(l)+H2O(l) ΔH=+131.4 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙两同学欲制取纯净的Fe(OH)2 ,根据如图所示的装置进行试验。A管中是Fe+H2SO4 , B管中是NaOH溶液,请回答下列问题。
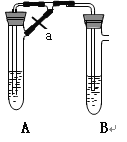
(1)同学甲:先夹紧止水夹a,使A管开始反应,在B管中观察到的现象是 。
(2)同学乙:打开a,使A管中反应一段时间再 夹紧止水夹a,实验中在B管中观察到的现象是 ,B中发生反应的离子方程式为
(3)同学乙打开a的目的 ; (填甲或乙)同学可成功。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是原子序数依次增大的短周期元素,且X、Z原子序数之和是Y、W原子序数之和的一半。甲、乙、丙、丁是由这些元素组成的二元化合物,M是某种元素对应的单质,乙和丁的组成元素相同,且乙是一种“绿色氧化剂”,化合物N在常温下是具有漂白性的气体。上述物质间的转化关系如图所示(部分反应物和生成物省略)。下列说法正确的是
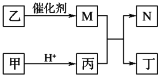
A.含W元素的盐溶液可能显酸性、中性或碱性
B.化合物N、乙烯均能使溴水褪色,且原理相同
C.元素的原子半径由大到小顺序: W > Z > Y > X
D.Y与Z、W形成的化合物中,各元素均满足8电子结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为不同温度下水的电离平衡曲线,已知pOH=lgc(OH),下列说法正确的是
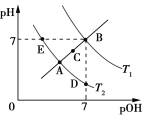
A. T1和T2的关系是:T1>T2
B. KW的关系是:B>C>A=D=E
C. A点到D点:加入少量酸可实现
D. T2时:pH=2的硫酸与pH=12的NaOH溶液等体积混合,溶液呈中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近,各国科学家联合成功研制的一种新型催化剂,可在常压下将二氧化碳与氢气的混合气体转化为甲烷,在容积为VL的容器中进行该转化,相关情况如图所示,下列有关说法不正确的是( )
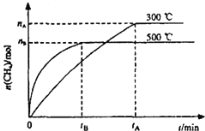
A.101kPa、120℃时,该反应的平衡常数表达式为K=![]()
B.断裂1mol C=O键、2mol H-H键所吸收的能量小于形成2mol C-H键、2mol O-H键所释放的能量
C.300℃时,从反应开始到达到平衡的这段时间,平均反应速率v(H2)=![]() mol/(L·min)
mol/(L·min)
D.其他条件不变,减小容器容积,二氧化碳的平衡转化率增大,平衡常数不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】银铜合金广泛用于航空工业。从切割废料中回收银并制备铜化工产品的工艺如下:

(注:Al(OH)3和Cu(OH)2受热易分解成对应的氧化物,且开始分解的温度分别为450℃和80℃)
(1)写出渣料与稀硫酸反应的化学方程式:________________________。
(2)固体混合物A的组成为 、 。
(3)操作A的名称为_______________。
(4)若银铜合金中铜的质量分数为64%,理论上5.0 kg废料中的铜可完全转化为 mol CuAlO2,至少需要1.0 molL—1的Al2(SO4)3溶液 L。
(5)CuSO4溶液也可用于制备胆矾晶体,其基本操作是 、 、过滤、干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z原子序数依次增大,并且位于三个不同的周期,W与Y同主族,X与Z的核外电子数之和是Y的核外电子数的2倍。化合物甲的结构如图所示,甲不溶于水,下列说法正确的是( )
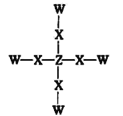
A.元素Z在自然界中既有游离态又有化合态
B.化合物甲中每个原子都满足8电子结构
C.W和Y形成二元化合物的熔点高于W和X形成二元化合物的熔点
D.元素的非金属性:Z>X>W>Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白杨素对肿瘤细胞有独特的杀伤作用,一种以甲苯、氯苯、丙烯酸为原料合成白杨素的路线如下:
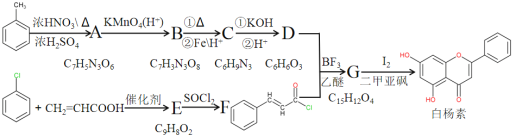
回答下列问题:
(1) A的名称是:__________________。
(2) C和D中不同化学环境的氢原子都为两种,则C和D的结构简式分别为:______、______。
(3) “D+F→G”的方程式为:_____________,物质E经“E→F”过程后再与D反应可大大减少副产物__________的生成。
(4) “G→白杨素”的反应类型为:_____________。试剂I2的选择是整个合成路线的关键。I2不能用更易结合H原子的Cl2替代的原因是:___________________。
(5) 下列关于白杨素的说法正确的是:_________。
A.白杨素的分子式C15H9O4
B.白杨素遇FeCl3溶液发生显色反应
C.与溴水反应,1mo白杨素最多消耗3molBr2
D.与足量H2发生加成反应后,白杨素分子中官能团种类减少1种
(6) E有多种同分异构体,满足分子中含有苯环,且能与4倍物质的量的银氨溶液反应的种类数有_________种,其中不同化学环境的氢原子有4种的结构简式为:______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com