
| A. | H2N-CH2-COOH既能与盐酸反应、又能与氢氧化钠溶液反应 | |
| B. | 油脂是高级脂肪酸甘油酯,均不能发生氢化反应 | |
| C. | 硫酸钠溶液和醋酸铅溶液均能使蛋白质变性 | |
| D. | 合成橡胶 的单体之一是2-丁炔 的单体之一是2-丁炔 |
分析 A.H2N-能与盐酸反应;-COOH能与氢氧化钠溶液反应;
B.有些油脂是不饱和高级脂肪酸的甘油酯;
C.重金属离子能使蛋白质变性而中毒;
D.若是加聚产物;找单体是在碳链两两(两个碳原子)断键,如链上有双键,则有四个碳原子断键(丁二烯结构).
解答 解:A.H2N-能与盐酸反应;-COOH能与氢氧化钠溶液反应,故A正确;
B.有些油脂是不饱和高级脂肪酸的甘油酯,能发生氢化反应,故B错误;
C.加入少量饱和的硫酸钠溶液会发生盐析,不发生变性,故C错误;
D.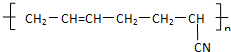 的单体是丁二烯和CH2=CH-CN,故D错误.故选A.
的单体是丁二烯和CH2=CH-CN,故D错误.故选A.
点评 本题考查油脂、蛋白质、氨基酸、高分子化合物的性质,难度中等,注意加聚产物找单体的方法:找单体是在碳链两两(两个碳原子)断键,如链上有双键,则有四个碳原子断键(丁二烯结构).


科目:高中化学 来源: 题型:多选题
| A. | Na2SO4溶液中混有少量CuSO4的杂质可用适量的KOH除去 | |
| B. | Na2CO3固体中含有少量NaHCO3杂质可用加热的方法提纯 | |
| C. | Fe(NO3)3中混有少量Fe(NO3)2的杂质可加入适量的氯水除去 | |
| D. | 可以用分液的方法分离CCl4和水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若c1=2c2,则w1<2w2,V<50 mL | B. | 若c1=2c2,则w1<2w2,V>50 mL | ||
| C. | 若w1=2w2,则c1<2c2,V=50 mL | D. | 若w1=2w2,则c1>2c2,V<50 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有②③④ | B. | 只有⑤⑦ | C. | 只有③④⑥⑦ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.6mol/L | B. | 2mol/L | C. | 2.8 mol/L | D. | 4 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某研究性学习小组欲测定室温下(25℃、101kPa)的气体摩尔体积,请回答以下问题.该小组设计的简易实验装置如图所示:该实验的主要操作步骤如下:
某研究性学习小组欲测定室温下(25℃、101kPa)的气体摩尔体积,请回答以下问题.该小组设计的简易实验装置如图所示:该实验的主要操作步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4 | B. | C2H4 | C. | C2H6 | D. | C3H8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com