
科目:高中化学 来源: 题型:
下列对化学反应的认识正确的是:
A.化学反应过程中,一定有化学键的断裂和形成
B.化学反应过程中,某离子被沉淀完全时,该离子在溶液中的浓度即为0
C.化学反应过程中,分子的种类和数目一定发生改变
D.放热反应的反应速率,一定比吸热反应的反应速率快
查看答案和解析>>
科目:高中化学 来源: 题型:
部分弱酸的电离平衡常数如下表:
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数 (25℃) | Ka=1.77×10-4 | Ka=4.9×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
下列选项正确的是[微软用户14]
A. 2CN-+H2O+CO2=2HCN+CO32-
B. 中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者小于后者
C. 物质的量浓度相等的HCOONa和KCN溶液中,c(Na+)-c(HCOO-) < c(K+)-c(CN-)
D. c(NH4+) 相等的HCOONH4溶液、NH4CN溶液、NH4HCO3溶液中,
c(NH4HCO3)>c(NH4CN) >c(HCOONH4)
查看答案和解析>>
科目:高中化学 来源: 题型:
合成氨工业上常用下列方法制备H2 :
方法: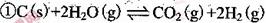
方法: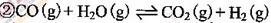
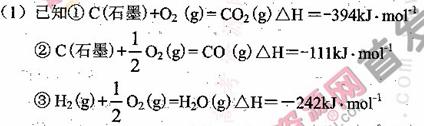
试计算25℃时由方法②制备l000g H2所放出的能量为_________ kJ。
(2)在一定的条件下,将C(s)和H2O(g)分别加入甲、乙两个密闭容器,发生反应:
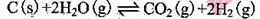 其相关数据如下表所示:
其相关数据如下表所示:
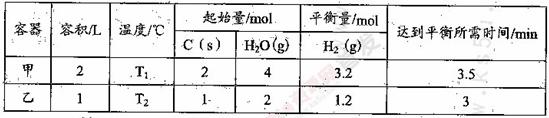
①T1_________T2 (填“>”、“=”或“<”);
T1℃时,该反应的平衡常数K=_________ 。
②乙容器中,当反应进行到1.5min时,H2O(g)的物质的量浓度范围是_________。
③一定条件下,在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是_________。
A.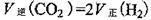
B混合气体的密度保持不变
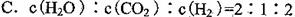
D.混合气体的平均相对分子质量保持不变
④某同学为了研究反应条件对化学平衡的影响,测得逆反应速率与时间的关系如图所示:
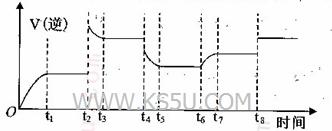
可见在t1、t3、t5、t7时反应都达了到平衡状态,如果t2、t4、t6、t8时都只改变了一个反应条件,则从t1到t8哪个时间段H2O (g)的平衡转化率最低_________,t4时刻改变的条件是__________。
⑤在25 ℃时,c mol/L,的醋酸与0.02mol/L NaOH溶液等体积混合后溶液刚好呈中性,
用含c的代数式表示CH3COOH的电离常数Ka=_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
能说明苯分子的平面六边形结构中,碳碳间不是单、双键交替的事实是( )
A.苯的二元取代物无同分异构体 B.苯的邻位二元取代物只有一种
C.苯的间位二元取代物只有一种 D.苯的对位二元取代物只有一种
查看答案和解析>>
科目:高中化学 来源: 题型:
镍氢电池的总反应式是H2+2NiO(OH) 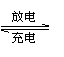 2Ni(OH)2,根据此反应式判断,此电池放电时,负极上发生反应的物质是( )。
2Ni(OH)2,根据此反应式判断,此电池放电时,负极上发生反应的物质是( )。
A.NiO(OH) B.Ni(OH)2 C.H2 D.H2和NiO(OH)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组性质比较中,正确的是 ( )
①酸性:HClO4>HBrO4>HIO4 ②碱性:Ba(OH)2>Mg(OH)2>Be(OH)2
③氧化性:F>C>O ④还原性:Cl<S<Si
⑤气态氢化物稳定性:HF>HCl>H2S
A、①②④⑤ B、②③④ C、 D、①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
已知25 ℃时有关弱酸的电离平衡常数如下表:
| 弱酸化学式 | HX | HY | H2CO3 |
| 电离平衡常数 | 7.8×10-9 | 3.7×10-15 | K1=4.3×10-7 K2=5.6×10-11 |
下列推断正确的是( )
A.HX、HY两种弱酸的酸性:HX>HY
B.相同条件下溶液的碱性:NaX>Na2CO3>NaY>NaHCO3
C.结合H+的能力:CO >Y->X->HCO
>Y->X->HCO
D.HX和HY酸性相同,都比H2CO3弱
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com