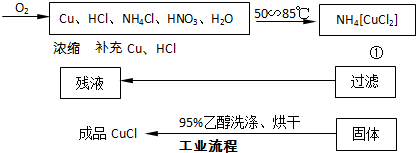
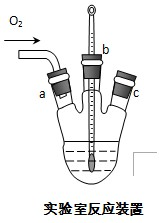
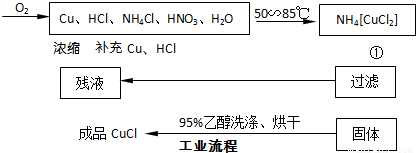
氯化亚铜在工业上应用广泛.氯化亚铜(CuC1)为白色晶体,微溶于水,能溶于氨水、浓盐酸,并生成配合物,不溶于硫酸、稀硝酸和醇.
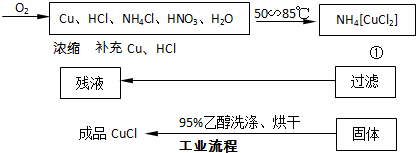
实验药品:铜丝20g、氯化铵20g、65% 硝酸10mL、36%盐酸15mL、水.
(1)反应①的化学方程式为
NH4[CuCl2]=CuCl↓+NH4Cl
NH4[CuCl2]=CuCl↓+NH4Cl
,用95%乙醇代替蒸馏水洗涤的主要目的是
避免CuCl溶于水而造成损耗或洗去晶体表面的杂质离子及水份
避免CuCl溶于水而造成损耗或洗去晶体表面的杂质离子及水份
.
(2)工业化生产时,95%乙醇可通过
蒸馏
蒸馏
方法回收并循环利用,而NH
4Cl、
HNO3
HNO3
(填化学式)可直接循环利用.
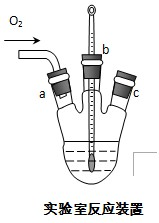
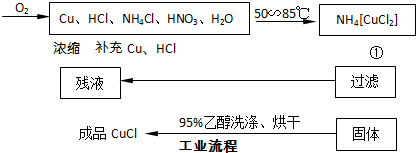
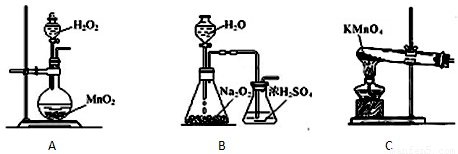
(3)实验室用右图装置制备CuC1.
①实验时通入O
2的速率不宜过大,为便于观察和控制产生O
2的速率,最宜选择
B
B
装置(填字母序号A、B、C).

②实验开始时,温度计显示反应液温度低于室温,主要原因是
氯化铵溶于水吸收大量热量,造成反应液温度降低
氯化铵溶于水吸收大量热量,造成反应液温度降低
;电炉加热升温至50℃时停止加热,反应快速进行,烧瓶上方气体颜色逐渐由无色变为红棕色,从环保角度考虑,当
烧瓶上方红棕色气体逐渐变为无色
烧瓶上方红棕色气体逐渐变为无色
_时才能停止通入氧气,待冷却至室温后,再打开瓶塞,沿
a或c
a或c
(填字母a、b、c)口倾出棕色反应液于1000mL大烧杯中,加水500mL,即刻有大量白色沉淀析出.