
| A. | 饱和氯水中Cl-、NO3-、Na+、SO32-可以大量存在 | |
| B. | 常温下干燥的Cl2能用钢瓶贮存,所以Cl2不与铁反应 | |
| C. | 向无色溶液中滴加氯水和CCl4,振荡,静置,下层溶液显紫色,说明原溶液中有I- | |
| D. | SO2通入碘水中,反应的离子方程式为SO2+I2+2H2O=SO32-+2I-+4H+ |
分析 A.饱和氯水具有强氧化性,能够氧化亚硫酸根离子;
B.氯气与铁加热反应生成氯化铁;
C.紫色的为碘单质,说明是碘离子被氧化成后生成的;
D.反应生成硫酸根离子,不是亚硫酸根离子.
解答 解:A.SO32-与氯水发生氧化还原反应,不能大量共存,故A错误;
B.铁与氯气能够发生反应:3Cl2+2Fe$\frac{\underline{\;点燃\;}}{\;}$2FeCl3,故B错误;
C.向无色溶液中滴加氯水和CCl4,振荡,静置,下层溶液显紫色,说明有碘单质生成,故原溶液中有I-,故C正确;
D.SO2通入碘水中,反应生成硫酸和碘化氢,正确的离子方程式为:SO2+I2+2H2O=SO42-+2I-+4H+,故D错误;
故选C.
点评 本题考查了离子方程式的书写,题目难度中等,注意掌握离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)等.


科目:高中化学 来源: 题型:选择题
| A. | 制普通玻璃的主要原料是纯碱、石灰石、石英 | |
| B. | 氨是制作氮肥、硝酸、铵盐的重要原料 | |
| C. | 将氢气和氯气混合光照生成氯化氢,溶于水制得盐酸 | |
| D. | 制造普通水泥的主要原料是黏土、石灰石 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单位时间生成nmol A的同时生成3n mol | |
| B. | B.容器内压强不随时间的变化而变化 | |
| C. | A,B,C的浓度相等的状态 | |
| D. | A,B,C的分子个数比为1:3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某同学组装了如图所示的电化学装置,电极ⅠAl,其它均为Cu,则下列正确的是( )
某同学组装了如图所示的电化学装置,电极ⅠAl,其它均为Cu,则下列正确的是( )| A. | 电流方向:电极Ⅳ→A→电极Ⅰ | B. | 电极Ⅰ发生还原反应 | ||
| C. | 电极Ⅱ逐渐溶解 | D. | 电极Ⅲ的电极反应:Cu2++2e-=Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
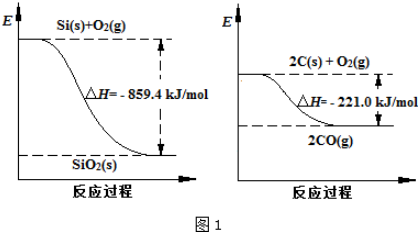
| 物质 | SiHCl3 | SiCl4 | AsCl3 |
| 沸点/℃ | 32.0 | 57.5 | 131.6 |
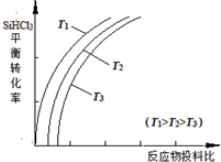
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 小于100 mL | B. | 200 mL | C. | 400 mL | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素Y的最高正化合价为+6 | |
| B. | 离子半径的大小顺序为W>Q>Z>X>Y | |
| C. | 气态氢化物的沸点:Y>W | |
| D. | 元素W的最高价氧化物对应的水化物酸性比Q的强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化性:H2SeO4>Cl2;H2SeO3>H2SO4 | |
| B. | 酸性:H2SO4>H2SeO4>H2SeO3 | |
| C. | 析出l mol硒需要消耗标准状况下22.4 L SO2 | |
| D. | 亚硒酸理论上既有氧化性,又有还原性,但还原性不及亚硫酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com