
| A. | 氮原子基态时电子排布式:1S22S22P3 | |
| B. | 右图为氮原子基态时的轨道表示式: | |
| C. | S2-电子排布式:1s22s22p63s23p4 | |
| D. | 29Cu原子基态排布式:[Ar]3d94s2 |
分析 A.氮原子为7号元素,原子核外有7个电子;
B.N原子核外有7个电子,分别位于1S、2S、2P轨道,应遵循保利原理和洪特规则即2p轨道3个电子自旋方向相同;
C.S原子为16号元素,S2-核外有18个电子;
D.Cu为29号元素,原子核外有29个电子,处于全满和半满的稳定结构;
解答 解:A.氮原子为7号元素,原子核外有7个电子,其核外电子排布式为:1s22s22p3,故A正确;
B.N原子核外有7个电子,分别位于1S、2S、2P轨道,应遵循保利原理和洪特规则即2p轨道3个电子自旋方向相同,其轨道表示式为 ,故B错误;
,故B错误;
C.S原子为16号元素,S2-核外有18个电子,其核外电子排布式为:1s22s22p63s23p6,故C错误;
D.Cu为29号元素,原子核外有29个电子,根据能量最低原理,处于全满和半满的稳定结构,其核外电子排布式为:1s22s22p63s23p63d104s1,故D错误;
故选:A.
点评 本题考查了原子的电子排布图以及电子排布式,明确相关化学用语的表示方法是解题关键,题目难度不大.


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:推断题
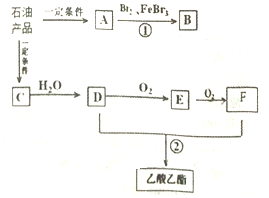 石油是一种重要的资源,其常压蒸馏的产品在一定条件下能转化为芳香烃.A-F均为有机化合物,C的产量可以用来衡量一个国家的石油化工发展水平.它们的转化关系如图所示(部分产物和反应条件已略去).
石油是一种重要的资源,其常压蒸馏的产品在一定条件下能转化为芳香烃.A-F均为有机化合物,C的产量可以用来衡量一个国家的石油化工发展水平.它们的转化关系如图所示(部分产物和反应条件已略去). ,反应类型为取代反应;
,反应类型为取代反应;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 20.0 mL 18 mol•L-1 H2SO4溶液 | B. | 250.0 mL 2 mol•L-1 HCl溶液 | ||
| C. | 150.0 mL 2 mol•L-1 H2SO4溶液 | D. | 500.0 mL 3 mol•L-1 HCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液c(H+)先变大后变小 | |
| B. | 溶液导电能力逐渐增强 | |
| C. | 氢硫酸完全反应生成1.6g硫 | |
| D. | 反应的离子方程式为:S2-+Cl2→2Cl-+S↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等质量的A、B两种烃分别完全燃烧后,生成的CO2与消耗的O2的物质的量均相同,则A和B一定互为同系物 | |
| B. | 沸点比较:正戊烷>异戊烷>新戊烷 | |
| C. | 邻二甲苯只有一种结构可以作为判断苯分子中不存在碳碳单键与碳碳双键的交替结构 | |
| D. | 煤炭经气化、液化和干馏等过程,可获得清洁能源和重要的化工原料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 卤素单质的熔沸点随原子序数增大而升高,所以碱金属单质熔沸点也随原子序数增大而升高 | |
| B. | Na能与冷水反应,推测Cs也能与冷水反应 | |
| C. | Fe与Cl2反应生成FeCl3,推测Fe与S反应生成Fe2S3 | |
| D. | CO2不能与Ba(NO3)2反应,所以SO2也不能与 Ba(NO3)2反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| SrSO4 | BaSO4 | SrCO3 | |
| Ksp | 3.2×10-7 | 1.1×10-10 | 1.6×10-10 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{6}^{12}$C与${\;}_{6}^{13}$ C | B. | CH4与CH3CH2CH3 | ||
| C. |  | D. |  |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com