
| A. | 分子式为C15H12O5 | |
| B. | 1molEGC与5molNaOH恰好完全反应 | |
| C. | 易发生氧化反应和取代反应,不能发生消去反应 | |
| D. | 遇FeCl3溶液能发生显色反应 |
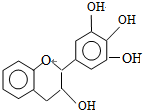
分析 根据有机物的结构简式判断有机物元素的种类和原子个数,可确定有机物的分子式,该有机物中含有酚羟基,可发生取代、显色反应,含有醇羟基,可发生消去、取代、氧化反应,以此解答该题.
解答 解:A.由有机物的结构简式可知该有机物的分子式为C15H14O5,故A错误;
B.酚羟基能和氢氧化钠反应,该分子中含有3个酚羟基,所以1molEGC与3molNaOH恰好完全反应,故B错误;
C.连接醇羟基碳原子相邻碳原子上含有氢原子,所以能发生消去反应,故C错误;
D.含有酚羟基,能和氯化铁发生显色反应,故D正确;
故选D.
点评 本题考查有机物结构和性质,为高频考点,侧重于有机物的官能团的性质的考查,难点是判断分子式,注意能发生消去反应醇的结构特点,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 它的元素符号为S | |
| B. | 它的核外电子排布式为1s22s22p63s23p4 | |
| C. | 可以与H2化合生成气态化合物 | |
| D. | 其轨道表示式为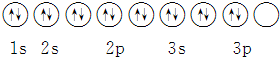 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
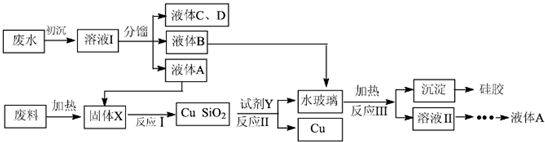
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
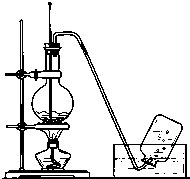 实验室常用如图所示装置制取乙烯,制取时:
实验室常用如图所示装置制取乙烯,制取时:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
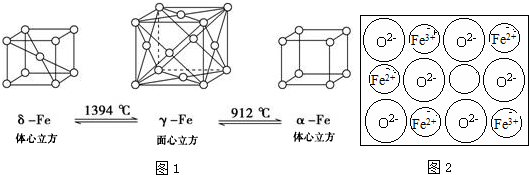
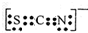 .Fe3+与SCN-可以形成配位数1~6的配离子,若Fe3+与SCN-以个数比1:5配合,则FeCl3与KSCN在水溶液中发生反应的化学方程式可以表示为FeCl3+5KSCN=K2[Fe(SCN)5]+3KCl.
.Fe3+与SCN-可以形成配位数1~6的配离子,若Fe3+与SCN-以个数比1:5配合,则FeCl3与KSCN在水溶液中发生反应的化学方程式可以表示为FeCl3+5KSCN=K2[Fe(SCN)5]+3KCl.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
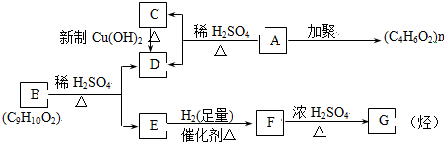
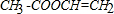 ,B:
,B: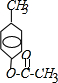 ;
;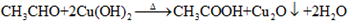 ,
,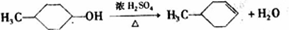 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜是一种紫红色金属 | |
| B. | 铜是热和电的良导体 | |
| C. | 铜是人类使用最早、应用最广泛的金属之一 | |
| D. | 铜在自然界中主要以单质的形式存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(H+)=c(OH-)的溶液中:SO42-、Na+、Cl-、Fe3+ | |
| B. | 在c(HCO3-)=0.1mol•L-1的溶液中:[Al(OH)4]-、Na+、NO3-、C6H5O- | |
| C. | 饱和氯水中:K+、Mg2+、CH3COO-、SO42- | |
| D. | 能使酚酞变红的溶液:Ba2+、NO3-、I-、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
;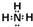 ;
;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com