
 +2H2O.
+2H2O. .
. .
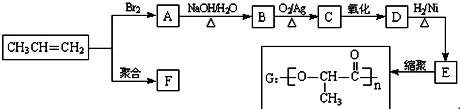
. 分析 丙烯与溴发生加成反应生成A为CH3CHBrCH2Br,A在氢氧化钠水溶液、加热条件下发生水解反应生成B为CH3CH(OH)CH2OH,B催化氧化生成C为 ,C氧化生成D为
,C氧化生成D为 ,D与氢气发生加成反应生成E为CH3CH(OH)COOH,E发生缩聚反应生成高聚物G,丙烯发生加聚反应生成高聚物F为
,D与氢气发生加成反应生成E为CH3CH(OH)COOH,E发生缩聚反应生成高聚物G,丙烯发生加聚反应生成高聚物F为 .
.
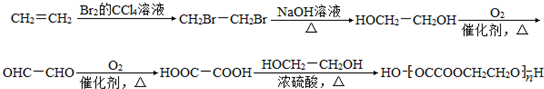
(5)乙烯与溴发生加成反应生成BrCH2CH2Br,在氢氧化钠水溶液、加热条件下发生取代反应生成HOCH2CH2OH,发生催化氧化生成OHC-CHO,再进一步氧化生成HOOC-COOH,最后HOOC-COOH与乙二醇在浓硫酸、加热条件下发生缩聚反应得到聚乙二酸乙二酯.
解答 解:丙烯与溴发生加成反应生成A为CH3CHBrCH2Br,A在氢氧化钠水溶液、加热条件下发生水解反应生成B为CH3CH(OH)CH2OH,B催化氧化生成C为 ,C氧化生成D为
,C氧化生成D为 ,D与氢气发生加成反应生成E为CH3CH(OH)COOH,E发生缩聚反应生成高聚物G,丙烯发生加聚反应生成高聚物F为
,D与氢气发生加成反应生成E为CH3CH(OH)COOH,E发生缩聚反应生成高聚物G,丙烯发生加聚反应生成高聚物F为 .
.
(1)B为CH3CH(OH)CH2OH,官能团的名称为羟基,故答案为:羟基;
(2)B转化为C的化学方程式是:CH3CH(OH)CH2OH+O2$→_{△}^{Ag}$ +2H2O,
+2H2O,
故答案为:CH3CH(OH)CH2OH+O2$→_{△}^{Ag}$ +2H2O;
+2H2O;
(3)在一定条件下,两分子CH3CH(OH)COOH能脱去两分子水形成一种六元环化合物,该化合物的结构简式是: ,
,
故答案为: ;
;
(4)E为CH3CH(OH)COOH,E一种同分异构体能发生银镜反应,说明含有醛基,1mol该种同分异构体与足量的金属钠反应产生1mol H2,还含有2个-OH,该同分异构体的结构简式为:HOCH2CH2(OH)CHO,
故答案为:HOCH2CH2(OH)CHO;
(5)乙烯与溴发生加成反应生成BrCH2CH2Br,在氢氧化钠水溶液、加热条件下发生取代反应生成HOCH2CH2OH,发生催化氧化生成OHC-CHO,再进一步氧化生成HOOC-COOH,最后HOOC-COOH与乙二醇在浓硫酸、加热条件下发生缩聚反应得到聚乙二酸乙二酯,合成路线流程图为: ,
,
故答案为: .
.
点评 本题考查有机物的推断与合成,利用顺推法结合物质的性质进行推断,是对有机化学知识的综合运用,需要学生熟练注意官能团的性质与转化,注意基础知识的全面掌握.


 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
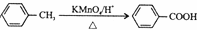
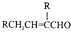
 .
. .
.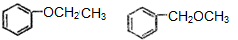 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向该溶液中加入过量NaOH溶液,仍能大量存在:ClO-、K+、CO32-、Cl- | |
| B. | 用明矾作净水剂:Al3++3H2O=Al(OH)3↓+3H+ | |
| C. | 向该溶液中加入过量Ba(OH)2溶液,有白色沉淀生成2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ | |
| D. | 将该溶液蒸干、灼烧得到是K 2SO4和Al2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
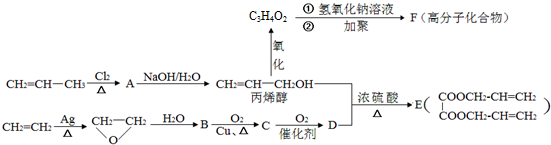
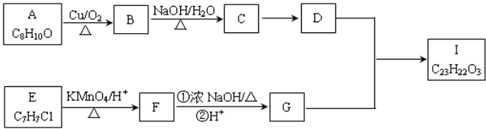
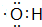 ;丙烯→A的反应类型为取代反应.
;丙烯→A的反应类型为取代反应.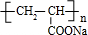 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | Z |
| W | ||
| T |
| A. | Y、W、T元素的原子半径及它们气态氢化物的还原性均依次递增 | |
| B. | Z氢化物的沸点一定比 X氢化物的沸点高 | |
| C. | X、Y元素形成的常见单质的化学键类型相同 | |
| D. | 根据元素周期律,可以推测存在化学式为T2Z3、X3Y4的两种物质,T元素存在同素异形现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
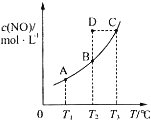 在容积一定的密闭容器中,置入一定量的一氧化氮和足量碳发生化学反应:
在容积一定的密闭容器中,置入一定量的一氧化氮和足量碳发生化学反应:| A. | 该反应的Q>0 | |
| B. | 若该反应在T1、T2时的平衡常数分别为K1、K2,则K1<K2 | |
| C. | 在T2时,若反应体系处于状态D,则此时V正>V逆 | |
| D. | 若状态B、C、D的压强分别为PB、PC、PD,则 PC=PD>PB |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
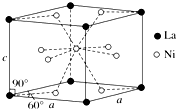 钛、铬、铁、镍、铜等金属及其化合物在工业上有重要用途.
钛、铬、铁、镍、铜等金属及其化合物在工业上有重要用途.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向NaHSO3溶液中通入NH3至中性,溶液中存在:c(NH4+)>c(SO32-) | |
| B. | NH4Cl和NH3•H2O混合液pH=7,一定存在c(NH4+)=c(Cl-) | |
| C. | NaHCO3溶液中存在HCO3-+H2O?H3O++CO32-,加水稀释后c(H+)减小 | |
| D. | pH相同的氯化铵与硫酸亚铁铵两种溶液中铵根离子浓度前者大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com