
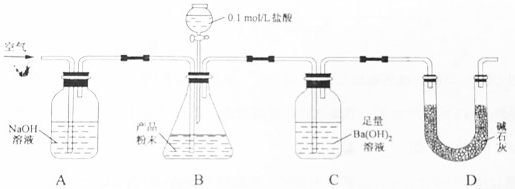
分析 以天然CaSiO3为吸收CO2制备CaCO3,产品中还含有少量CaSiO3和SiO2杂质,为测定产品中CaCO3的含量,利用装置A中氢氧化钠溶液吸收空气中的二氧化碳,防止干扰测定结果,装置B中加入盐酸和样品中碳酸钙反应生成二氧化碳通过装置C吸收,称量装置C质量增加测定生成的二氧化碳计算碳酸钙含量,装置D是防止空气中的二氧化碳进入装置C影响测定结果,
(1)装置A是开始除去空气中的二氧化碳,反应完后把生成的二氧化碳气体赶入装置C中完全吸收;实验过程中需缓缓通入空气是排除装置中空气,赶出生成的二氧化碳完全被氢氧化钡溶液吸收;
(2)据实验操作的步骤以及每步操作需要仪器确定反应所需仪器;
(3)B中的反应是CaSiO3和盐酸反应生成硅酸沉淀和氯化钙,碳酸钙和盐酸反应生成氯化钙、二氧化碳和水,水蒸气、HCl气体会进入装置C中使得CO2称量结果偏大,故测定装置C在吸收CO2前后质量差不能准确得到碳酸钙含量;
(4)如果没有D装置.空气中二氧化碳会进入装置C,导致测定二氧化碳质量增大.
解答 解:(1)利用装置A中氢氧化钠溶液吸收空气中的二氧化碳,防止干扰测定结果,装置B中加入盐酸和样品中碳酸钙反应生成二氧化碳通过装置C吸收,称量装置C质量增加测定生成的二氧化碳计算碳酸钙含量,装置D是防止空气中的二氧化碳进入装置C影响测定结果,
故答案为:开始除去空气中的二氧化碳,反应完后把生成的二氧化碳气体赶入装置C中完全吸收;赶净装置中的空气,把生成的二氧化碳气体全部赶入装置C中氢氧化钡溶液完全吸收;
(2)操作步骤有计算、量取、稀释、移液、洗涤移液、定容、摇匀等操作,用量筒量取(用到胶头滴管)浓盐酸,在烧杯中稀释,用玻璃棒搅拌,冷却至室温后转移到250mL容量瓶中,并用玻璃棒引流,洗涤2-3次,将洗涤液转移到容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加至溶液凹液面与刻度线水平相切,盖好瓶塞颠倒摇匀.
所以需要的仪器为:玻璃棒、烧杯、胶头滴管、量筒、250mL容量瓶,
故答案为:胶头滴管;250mL容量瓶;
(3)B中主要反应的离子方程式为CaSiO3和盐酸反应生成硅酸沉淀和氯化钙,碳酸钙和盐酸反应生成氯化钙、二氧化碳和水,水蒸气,反应的离子方程式为:CaSiO3+2H+=Ca2++H2SiO3↓,CaCO3+2H+=Ca2++CO2↑+H2O,水蒸气、HCl气体会进入装置C中使得CO2称量结果偏大,故测定装置C在吸收CO2前后质量差不能准确得到碳酸钙含量,需要在装置B、C间添加吸收HCl的装置,
故答案为:CaSiO3+2H+=Ca2++H2SiO3↓,CaCO3+2H+=Ca2++CO2↑+H2O;有;水蒸气、HCl气体会进入装置C中使得CO2称量结果偏大;
(4)如果没有D装置.空气中二氧化碳会进入装置C,导致测定二氧化碳质量增大,则测定的CaCO3的含量将偏大,
故答案为:偏大.
点评 本题考查学生对实验设计的能力、对操作的评价、物质含量的测定、化学计算等,根据物质的化学性质,要认真分析,把握实验设计的每个步骤中的实验目的,难度中等.


 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:选择题
| 晶体 | NaCl | MgCl2 | AlCl3 | SiCl4 | 单质R |
| 熔点 | 810℃ | 710℃ | 180℃ | -70℃ | 2300℃ |
| 沸点 | 1465℃ | 1418℃ | 177.8℃ | 57℃ | 2500℃ |
| A. | AlCl3为离子晶体 | B. | MgCl2为离子晶体 | ||
| C. | SiCl4是分子晶体 | D. | 单质R可能是原子晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 加入少量稀硫酸 | B. | 加热 | ||
| C. | 加蒸馏水 | D. | 加入少量硫酸铜溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2(OH)CH2OH和乙醇是同系物 | |
| B. | 正丁烷与异丁烷互为同分异构体,金刚石与石墨也是 | |
| C. | 丙烯与水加成有2种同分异构体产物 | |
| D. | SiO2既可以和NaOH溶液反应,又可以与氢氟酸反应,所以其为两性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
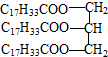 .从酯的性质看,油脂A在酸性条件下和碱性条件下均能发生水解,水解的共同产物是
.从酯的性质看,油脂A在酸性条件下和碱性条件下均能发生水解,水解的共同产物是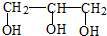 (写结构简式).
(写结构简式).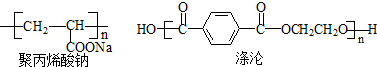
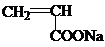 ,反应类型是加聚反应;
,反应类型是加聚反应;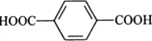 ,其核磁共振氢谱的峰面积比是1:2(或2:1).
,其核磁共振氢谱的峰面积比是1:2(或2:1).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | OH-、SO42-、S 2- | B. | OH-、S 2-、CO3 2- | ||
| C. | OH-、CO3 2-、SO4 2- | D. | SO4 2-、S 2-、CO3 2- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.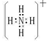 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④⑥⑦ | B. | ②③⑤⑦ | C. | ②⑤⑦ | D. | ②④⑤⑦ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com