
分析 (1)硫杆菌存在时,FeSO4被氧化的速率是无菌时的5×105倍,说明硫杆菌做反应的催化剂加快反应速率;
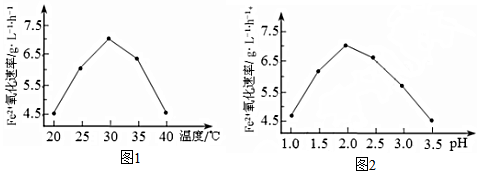
(2)从图象中分析可知,使用硫杆菌的最佳条件是亚铁离子氧化速率最大时,反应温度过高,反应速率下降是因为升温使蛋白质发生变性;
(3)当n(H2O2)/n(H2S)=4时,结合氧化还原反应电子守恒,4H2O2~4H2O~8e-,电子守恒得到H2S变化为+6价化合物;
(4)过程①是二氧化硫和氢氧化钠溶液反应生成亚硫酸钠和水;过程②NaOH再生是平衡CaO(s)+H2O (l)═Ca(OH)2(s)?Ca2+(aq)+2OH-(aq)正向进行;氢氧根离子浓度增大;
(5)NH3•H2O的Kb=1.8×10-5,若氨水的浓度为2.0mol•L-1,可结合Kb=$\frac{c(N{{H}_{4}}^{+})c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$计算c(OH-),H2SO3的Ka2=6.2×10-8,结合Ka2=$\frac{c(S{{O}_{3}}^{2-})c({H}^{+})}{c(HS{{O}_{3}}^{-})}$计算c(SO32-)/c(HSO3-).
解答 解:(1)4FeSO4+O2+2H2SO4$\frac{\underline{\;硫杆菌\;}}{\;}$2Fe2(SO4)3+2H2O,硫杆菌存在时,FeSO4被氧化的速率是无菌时的5×105倍,该菌的作用是做催化剂降低反应的活化能,
故答案为:降低反应活化能(或作催化剂);
(2)从图象中分析可知,使用硫杆菌的最佳条件是亚铁离子氧化速率最大时,需要的温度和溶液PH分别为:30℃、pH=2.0,反应温度过高,反应速率下降是因为升温使蛋白质发生变性,催化剂失去生理活性,
故答案为:30℃、pH=2.0; 蛋白质变性(或硫杆菌失去活性);
(3)当$\frac{n({H}_{2}{O}_{2})}{n({H}_{2}S)}$=4时,结合氧化还原反应电子守恒,4H2O2~4H2O~8e-,电子守恒得到H2S变化为+6价化合物,H2S~H2SO4~8e-,氧化产物的分子式为H2SO4,
故答案为:H2SO4 ;
(4)过程①是二氧化硫和氢氧化钠溶液反应生成亚硫酸钠和水,反应的离子方程式为:2OH-+SO2=SO32-+H2O,过程②加入CaO,存在CaO(s)+H2O (l)═Ca(OH)2(s)?Ca2+(aq)+2OH-(aq),因SO32-与Ca2+生成CaSO3沉淀,平衡向正向移动,有NaOH生成,
故答案为:2OH-+SO2=SO32-+H2O;SO32-与Ca2+生成CaSO3沉淀,平衡向正向移动,有NaOH生成;
(5)NH3•H2O的Kb=1.8×10-5,若氨水的浓度为2.0mol•L-1,由Kb=$\frac{c(N{{H}_{4}}^{+})c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$可知c(OH-)=$\sqrt{1.8×1{0}^{-5}×2}$mol/L=6.0×10-3mol/L,
当c(OH-)降至1.0×10-7 mol•L-1时,c(H+)=1.0×10-7 mol•L-1,H2SO3的Ka2=6.2×10-8,由Ka2=$\frac{c(S{{O}_{3}}^{2-})c({H}^{+})}{c(HS{{O}_{3}}^{-})}$可知c(SO32-)/c(HSO3-)=$\frac{6.2×1{0}^{-8}}{1×1{0}^{-7}}$=0.62,
故答案为:6.0×10-3;0.62.
点评 本题考查较为综合,涉及弱电解质的电离以及二氧化硫的污染和治理,为高考常见题型和高频考点,侧重考查学生的分析能力和计算能力,注意把握题给信息的分析,掌握电离平衡常数的运用,难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| 实验 | 结论 | |
| A. | 将乙烯通入溴的四氯化碳溶液,溶液最终变为无色透明 | 生成的1,2-二溴乙烷无色、可溶于四氯化碳 |
| B. | 乙醇和水都可与金属钠反应产生可燃性气体 | 乙醇分子中的氢与水分子中的氢具有相同的活性 |
| C. | 用乙酸浸泡水壶中的水垢,可将其清除 | 乙酸的酸性小于碳酸的酸性 |
| D. | 甲烷与氯气在光照下反应后的混合气体能使湿润的石蕊试纸变红 | 生成的氯甲烷具有酸性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
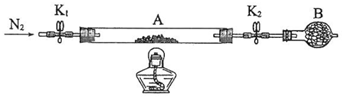
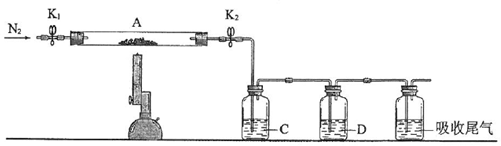
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
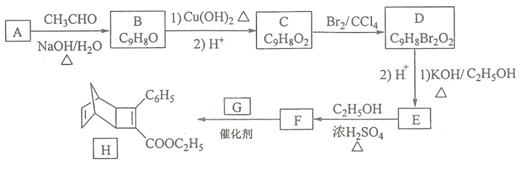
 +
+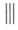 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$
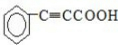 .
.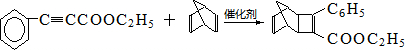 .
.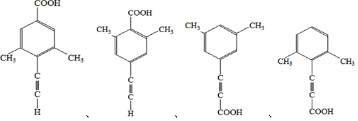 .
.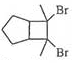 的合成路线
的合成路线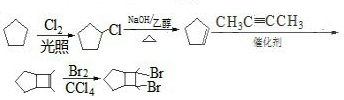 (其他试剂任选).
(其他试剂任选).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠与水反应:Na+2H2O═Na++2OH-+H2↑ | |
| B. | 电解饱和食盐水获取烧碱和氯气:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2↑+2OH- | |
| C. | 向氢氧化钡溶液中加入稀硫酸:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| D. | 向碳酸氢铵溶液中加入足量石灰水:Ca2++HCO3-+OH-═CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 平衡正向移动 | B. | B的浓度增大 | C. | A的浓度减小 | D. | 逆反应速率加快 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 操作和现象 | 结论 |
| A. | 滴有酚酞的Na2CO3溶液中加入BaCl2溶液,红色变浅 | Na2CO3溶液中存在水解平衡 |
| B. | 向电石中加入饱和食盐水制乙炔,并将产生的气体直接填入酸性高锰酸钾溶液中,溶液紫红色褪去 | 记明乙炔能被酸性高锰酸钾氧化 |
| C. | 常温下,测得饱和Na2S溶液的PH大于饱和Na2CO3溶液 | 常温下水解程度:S2->CO32- |
| D. | 向分液漏斗中加入碘水后再加入CCl4,充分振荡,分层,且上层溶液至紫色 | CC14可作为碘的萃取剂 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:r(X)>r(R)>r(W) | |
| B. | X与Y只能形成一种化合物 | |
| C. | X的简单气态氢化物的热稳定性比Z的弱 | |
| D. | 由W、R、X三种元素组成的化合物可以是酸、碱或盐 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com