
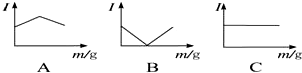
���� ��Һ��������������Ũ�ȳ����ȣ����ɳ����ȣ�������ǿ���أ�
A����Һ����������������С����A��Һ������Ũ����������С��
B����Һ���������ȼ�С��������B��Һ������Ũ���ȼ�С������
C����Һ�����������䣬˵��C��Һ������Ũ�Ȳ��䣬�ݴ˷������
��� �⣺��Һ��������������Ũ�ȳ����ȣ����ɳ����ȣ�������ǿ���أ�
A����Һ����������������С����A��Һ������Ũ����������С��
B����Һ���������ȼ�С��������B��Һ������Ũ���ȼ�С������
C����Һ�����������䣬˵��C��Һ������Ũ�Ȳ��䣬
A���÷�Ӧ����ʽΪBa2++2OH-+2H++SO42-=BaSO4��+2H2O������ϡ����ļ��룬����Ũ�ȼ�С��������ǡ�÷�Ӧʱ����Ũ����С����Һ����������С����������ϡ����ʱ������Ũ��������Һ������������
B�����ӷ�Ӧ����ʽΪCH3COOH+NH3��H2O=NH4++CH3COO-������һˮ�ϰ��ļ��룬����Ũ��������Һ��������������ǡ�÷�Ӧʱ��Һ����������������백ˮ������Ũ�ȼ�С����Һ����������С��
C�����ӷ�Ӧ����ʽΪCa2++2OH-+CO2=CaCO3��+H2O�����Ŷ�����̼��ͨ�룬����Ũ�ȼ�С����Һ�����������ͣ�����ǡ�÷�Ӧʱ����Ũ����С����Һ����������ͣ�����ͨ�������̼�����߷�Ӧ���ɿ�����ǿ����ʣ�CaCO3+H2O+CO2=Ca��HCO3��2������Ũ��������Һ����������ǿ��
D�����ӷ�Ӧ����ʽΪNH4++OH-=NH3��H2O������NaOH�ļ��룬����Ũ�Ȼ������䣬������Һ���������������䣻
ͨ�����Ϸ���֪����Aͼ�仯����һ�µ���B����Bͼ�仯����һ�µ���AC����Cͼ�仯����һ�µ���D��
�ʴ�Ϊ��B��AC��D��
���� ���⿼����Һ��������ͼ�������Ϊ��Ƶ���㣬��ȷ��Һ������ǿ��������Ũ�ȹ�ϵ�ǽⱾ��ؼ���ע����Һ������ǿ��������ǿ���أ���Ŀ�ѶȲ���


 ��ʦָ����ĩ��̾�ϵ�д�
��ʦָ����ĩ��̾�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ﵽƽ��ʱ��N2��H2��ת����֮��Ϊ1��1 | |
| B�� | 10������v��H2��=0.35mol/��L•min�� | |
| C�� | ƽ����������ܶ�Ϊ124g/L | |
| D�� | ƽ���������У�n��N2����n��H2����n��NH3��=1��3��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| ���� | �۸�/Ԫ?��-1 |
| ƯҺ����25.2%NaClO�� | 450 |
| ˫��ˮ����30%H2O2�� | 2400 |
| �ռ��98%NaOH�� | 2100 |
| �����99.5%Na2CO3�� | 600 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ұ��� | B�� | ���ұ��� | C�� | ���Ҷ��� | D�� | �Ҷ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Cu2+ | B�� | Cl- | C�� | Na+ | D�� | Ba2+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
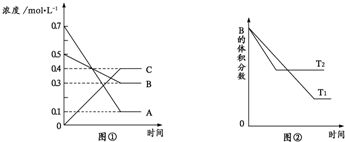
| A�� | �÷�Ӧ�Ļ�ѧ����ʽ��A+3B�T2C | |
| B�� | �÷�Ӧ������ӦΪ���ȷ�Ӧ | |
| C�� | ���������£����������ܶȲ��ٱ仯����֤���÷�Ӧ�ﵽƽ�� | |
| D�� | ѹǿ������÷�Ӧ������Ӧ���������淴Ӧ���ʼ�С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Һ����������Ϊ7.8% | B�� | ��Һ�����ʵ���������7.8g | ||
| C�� | ��Һ��ˮ����������92.2g | D�� | ��Һ����������100g |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com