
短周期元素X、Y、Z、W原子序数依次增大,X原子2p能级的3个轨道上都有电子且轨道上有2个未成对电子,Y与X可形成Y2X2和Y2X两种离子化合物,Z原子的核外电子数比Y原子多1,W与X同主族。下列说法正确的是( )
A. 元素的非金属性:X<W
B. 原子半径:Y<Z<W
C. 单质的还原性:Y>Z
D. Y和Z两者最高价氧化物对应的水化物能相互反应
科目:高中化学 来源:2016-2017学年吉林省高一上学期期末化学试卷(解析版) 题型:选择题
在FeCl3、CuCl2和HCl的混合溶液中加入铁粉,待反应结束后,将剩余的固体滤出,发现固体能被 磁铁吸引,则反应后溶液中大量存在的阳离子是
磁铁吸引,则反应后溶液中大量存在的阳离子是
A.Fe2+ B.H+ C.Cu2+和Fe 2+ D.Fe3+和Cu2+
2+ D.Fe3+和Cu2+
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省乐山市高一上学期教学质检化学试卷(解析版) 题型:推断题
(6分)A、B、C、D、E五种物质中均含有同一种元素,其相互转化关系如下图所示:
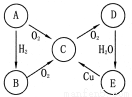
请回答下列问题:
(1)如果A是淡黄色固体,则B是(写化学式,下同) ,E是 。
(2)如果A是无色气体:B→C的化学方程式为 ;E→C的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省乐山市高一上学期教学质检化学试卷(解析版) 题型:选择题
下列不涉及氧化还原反应的是( )
A.钢铁生锈 B.用铂丝蘸取NaCl溶液进行焰色反应
C.自然界中“氮的固定 ” D.铜铸塑像上出现铜绿[Cu2(OH)2CO3]
” D.铜铸塑像上出现铜绿[Cu2(OH)2CO3]
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省乐山市高二上学期教学质检化学试卷(解析版) 题型:填空题
(1)下列7种物质:
①白磷(P4) ②水晶 ③氯化铵 ④氢氧化钙 ⑤氟化钠 ⑥过氧化钠 ⑦干冰
固态时都为晶体,其中既有范德华力,又有非极性键的晶体是 (填写序号,下同),只存在离子键的是 ,熔化时只破坏共价键的是 。
(2)下图是XeF4的结构示意图,据此判断XeF4是 (填“极性”、“非极性”)分子。
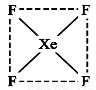
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省乐山市高二上学期教学质检化学试卷(解析版) 题型:选择题
只有阳离子而没有阴离子的晶体是( )
A.金属晶体 B.原子晶体 C.离子晶体 D.分子晶体
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省等三校高二上第二次联考化学试卷(解析版) 题型:填空题
铜及其化合物在工农业生产及日常生活中应用非常广泛。回答下列问题:
(1)纳米级Cu2O由于具有优良的催化性能而受到关注,制取Cu2O的两种方法如下表所示。
方法I | 用炭粉在高温条件下还原CuO生成Cu2O和CO2 |
方法II | 用肼(N2H4)还原新制Cu(OH)2 |
① 方法I中还原剂与氧化剂的物质的量之比为________。
② 方法II发生反应的化学方程式为______________。
(2)氢化亚铜是一种红色同体,可由下列反应制备:
4CuSO4+3H3PO2+6H2O=4CuH↓+4H2SO4+3H3PO4
该反应中每转移3 mol电子,生成CuH的物质的量为___________mol。
(3)氯化铜溶液中各种含铜微粒的分布分数(平衡时某微粒的浓度占各微粒浓度之和的分数)与c(C1-)之间的关系如图所示。
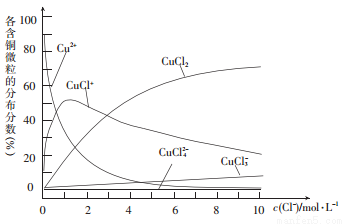
① 当c(C1-)= 9 mol/L时,溶液中3种主要含铜微粒浓度的大小关系为__________。
② 在c(C1-)= l mol /L的氯化铜溶液中,加人AgNO3溶液,CuCl+转化为Cu2+的离子方程式为____________。
(4)已知:Cu(OH)2是二元弱碱,25℃时Ksp[Cu(OH)2]=2.0×10-20。则此温度下在铜盐溶液中Cu2+发生水解反应的平衡常数为______________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省等三校高二上第二次联考化学试卷(解析版) 题型:选择题
只用NaOH溶液不能除去下列各组物质中的杂质(括号内为杂质)的是
A.Mg(Al2O3) B.MgCl2(A1Cl3) C.Mg(Si) D.MgO(SiO2)
查看答案和解析>>
科目:高中化学 来源:2017届福建省宁德市高三上学期单科质检模拟化学试卷(解析版) 题型:实验题
为探究某铁碳合金与浓硫酸在加热条件下的反应的部分产物并测定铁碳合金中铁元素的质量分数,某化学活动小组设计了如图所示的实验装置,并完成以下实验探究。
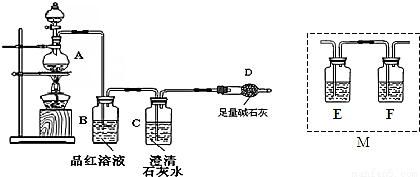
(1)往圆底烧瓶中加入m g铁碳合金,并滴入过量浓硫酸,未点燃酒精灯前,A、B均无明显现象,其原因是:①常温下碳与浓硫酸不反应;② 。
(2)点燃酒精灯,反应一段时间后,从A中逸出气体的速率仍然较快,除因反应温度较高外,还可能的原因是 。
(3)装置B的作用是 。
(4)甲同学观察到装置C中有白色沉淀生成,他得出了使澄清石灰水变浑浊的气体是二氧化碳。装置A中能产生二氧化碳的化学方程式为 。
(5)乙同学认为甲同学的结论是错误的,他认为为了确认二氧化碳的存在,需在装置B-C之间添加装置M。装置E、F中盛放的试剂分别是 、 。重新实验后观察到装置F中的现象是 。
(6)有些同学认为合金中铁元素的质量分数可用KMnO4溶液来测定。(5Fe2+ + MnO4- + 8H+=5Fe3+ + Mn2+ + 4H2O)。测定铁元素质量分数的实验步骤如下:
Ⅰ.往烧瓶A中加入过量铜使溶液中的Fe3+完全转化为Fe2+,过滤,得到滤液B;
Ⅱ.将滤液B稀释为250mL;
Ⅲ.取稀释液25.00mL,用浓度为c mol·L-1的酸性KMnO4溶液滴定,三次滴定实验所需KMnO4溶液体积的平均值为V mL。
① 步骤Ⅱ中,将滤液B稀释为250mL需要用到的玻璃仪器除烧杯、玻璃棒、胶头滴管外,还必须要用到的是 。
② 判断滴定终点的标志是 。
③ 铁碳合金中铁元素的质量分数为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com