
(提前进度)
(1)已知H2O(1)=H2O(g);△H=+44KJ/mol。在25℃、101 kPa下,1g甲醇燃烧生成CO2和气态水时放热19.93kJ,则该反应的热化学方程式应为______。
(2)已知H2的燃烧热△H=-285.8kJ·mol-1,CO的燃烧热△H=-282.8 kJ·mol-1。现有CO、H2、CO2组成的混合气体67.2L(标准状况),经充分燃烧后放出的总热量为710.0 kJ,并生成18g液态水,求燃烧前混合气体中CO的体积分数。
(1)CH3OH(l)+3/2O2(g)=(g)CO2(g)+2H2O(l) △H=-725.76kJ/mol (3分)
(2)50%
【解析】(1)1g甲醇燃烧生成CO2和气态水时放热19.93kJ,则1mol甲醇燃烧燃烧非常的热量是19.93kJ×32=637.76kJ。生成的2mol气态水变成液态水,又放出44kJ×2=88kJ,所以总共放出的热量是637.76kJ+88kJ=725.76kJ,所以热化学方程式为
CH3OH(l)+3/2O2(g)=(g)CO2(g)+2H2O(l) △H=-725.76kJ/mol 。
(2)考查根据方程式进行的有关计算。
(2)标准状况下n(混合气体)= =3
mol(1分)
=3
mol(1分)
其中有n(H2)=  =1 mol (2分)
=1 mol (2分)
1mol H2燃烧生成液态水时放热 =285.8kJ(1分)
=285.8kJ(1分)
CO燃烧时放出的热量为710.0kJ-285.8kJ=424.2kJ(CO2不燃烧)(1分)
故n(CO)=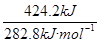 =1.5mol(1分)
=1.5mol(1分)
CO的体积分数为 ×100%=50% (1分)
×100%=50% (1分)


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源:四川省广元中学2009-2010学年高二下学期开学考试化学试题 题型:058
(教学进度没有提前学校的学生做)某学习小组用如图装置测定铝镁合金中铝的相对原子质量.

(1)A的仪器名称为________,A中试剂为________.
(2)检查装置不漏气后将药品和水装入各仪器中,连接好装置后,需进行的操作还有:①记录反应前C的液面位置;②将B中剩余固体过滤、洗涤、干燥、称重;③待B中不再有气体产生并恢复至室温后,记录C的液面位置;④由A向B中滴加足量试剂.上述操作的顺序是________(填序号).
上述操作③在记录C的液面位置时,除视线平视外,还应________.
(3)B中发生反应的化学方程式为________.
(4)若实验用铝镁合金的质量为a g,测得氢气体积为b mL(已换算为标准状况),B中剩余固体质量为c g,则铝的相对原子质量为________.
(5)实验过程中,若未洗涤过滤所得的不溶物,则测得铝相对原子质量将________(填“偏大”、“偏小”或“不受影响”)
(6)有同学提出应在装置(Ⅰ)(Ⅱ)之间添加一个装有浓H2SO4的洗气瓶,你认为有必要吗?________(填“有”或“无”)
查看答案和解析>>
科目:高中化学 来源:2011-2012学年江西省吉安市高一下学期期末教学质量评价化学试卷(带解析) 题型:计算题
(提前进度)
(1)已知H2O(1)=H2O(g);△H=+44KJ/mol。在25℃、101 kPa下,1g甲醇燃烧生成CO2和气态水时放热19.93kJ,则该反应的热化学方程式应为______。
(2)已知H2的燃烧热△H=-285.8kJ·mol-1,CO的燃烧热△H=-282.8 kJ·mol-1。现有CO、H2、CO2组成的混合气体67.2L(标准状况),经充分燃烧后放出的总热量为710.0 kJ,并生成18g液态水,求燃烧前混合气体中CO的体积分数。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com