
| ���� | CH3OH | CH3OCH3 | H2O |
| Ũ��/��mol?L-1�� | 0.44 | 0.6 | 0.6 |
| c(CH3OCH3)��c(H2O) |
| c2(CH3OH) |
| 0.6��0.6 |
| 0.442 |
| (0.6+x)2 |
| (0.44-2x)2 |
| 1.6mol/L |
| 10min |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Ħ����������1 mol���ʵ����� |
| B��1 mol CO2������Ϊ44 g?mol-1 |
| C�����ʵ����������ʵĺ�������������ӵ���Ŀ��ϵ���� |
| D��Ħ���ǹ��ʿ�ѧ�罨����õ�һ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ڡ��о���Ӧ���ʵ�Ӱ�����ء�ʵ���У�Na2S2O3+H2SO4=Na2SO4+S+SO2+H2O����ͨ���۲�������ݵĿ������Ƚϲ�ͬ�����¸÷�Ӧ�����ʴ�С |
| B��Ϊ�˾�ȷ�ⶨ����������������Һ��Ӧ�ķ�Ӧ�ȣ�������Ϻ�������ȡ�¶ȼƵĶ�������ֹ����ɢʧ |
| C�������ۡ�̼�ۡ������Ȼ��ƺ�ˮ��Ϸ������ϴ��д��࣬���ִ�����о������ȣ���������������� |
| D������к͵ζ�ʵ���У��յ��жϹ��٣����±�Һ�ζֻ࣬�����µζ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
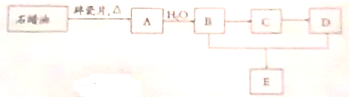
 ij��ѧ�о�С��Ϊ��̽������������̷�Ӧ����������Ũ�ȣ��������ͼ��ʾ��ʵ��װ�ã���Բ����ƿ�м���20mL 12mol?L-1Ũ����������������̷�ĩ�����ȣ���֪װ��B��C�е��Լ����������������Ƿ�Ӧ��������ƿ����Һ����ı仯��
ij��ѧ�о�С��Ϊ��̽������������̷�Ӧ����������Ũ�ȣ��������ͼ��ʾ��ʵ��װ�ã���Բ����ƿ�м���20mL 12mol?L-1Ũ����������������̷�ĩ�����ȣ���֪װ��B��C�е��Լ����������������Ƿ�Ӧ��������ƿ����Һ����ı仯���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ѡ�� | ʵ�����ģ�ʡ�Լг�װ�ã� | ��Ӧʵ�� |
| A | �����ƾ��� | ����NaCl��Һ�õ����� |
| B | ©������ֽ | ��CaCO3��Һ�з����CaCO3 |
| C | ������ƽ����ͷ�ι� | ��NaCl��������1mol?L-1����Һ |
| D | ��Һ©�� | ��CCl4��ȡ��ˮ�еĵ� |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������������ʯΪԭ�ϣ��ڸ�����������CO��ԭ�õ������� |
| B����þ���ú�ˮΪԭ�ϣ���һϵ�й����Ƶ�����þ���壬������ڵ�����þ�õ�þ���� |
| C�����ƣ��ú�ˮΪԭ���Ƶþ��Σ��ٵ�ⴿ����NaCl��Һ�õ������� |
| D�����������������У���һϵ�з�Ӧ�õ��Ȼ�����������ڵ��Ȼ����õ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 1 |
| 2 |
| 3 |
| 2 |
| A��K1=K2 |
| B��K22=K1 |
| C��K12=K2 |
| D����ȷ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com