
| A、硫酸的摩尔质量与NA个硫酸分子的质量在数值上相等 |
| B、NA个氧分子与NA个氢分子的质量比等于16:1 |
| C、0.1mol/L 的NaCl溶液中,Na+与Cl-离子总数为0.2NA |
| D、标准状况下,0.5NA个氯分子所占体积为11.2L |


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol?L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
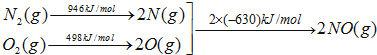
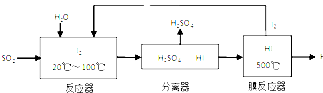
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(OH-)=c(HS-)+c(H+)+c(H2S) |
| B、c(OH-)=c(HS-)+c(H+)+2 c(H2S) |
| C、c(Na+)=c(S2-)+c(HS-)+c(H2S) |
| D、c(Na+)+c (H+)=c(HS-)+c(OH-)+c(S2-) |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铁片上镀锌的阴极 |
| B、电解氯化铜溶液时的阴极 |
| C、电解食盐水时的阴极 |
| D、铜锌原电池的负极(硫酸溶液为电解质) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、AB2 |
| B、AB2 |
| C、A2B2 |
| D、A3B2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
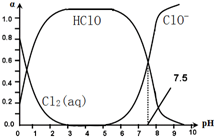 氯在饮用水处理中常用作杀菌剂,且HClO的杀菌能力比ClO-强.25℃时氯气-氯水体系中存在以下平衡关系:
氯在饮用水处理中常用作杀菌剂,且HClO的杀菌能力比ClO-强.25℃时氯气-氯水体系中存在以下平衡关系:| A、氯处理饮用水时,在冬季的杀菌效果比在夏季好 |
| B、25℃时,HClO的电离常数Ka=10-7.5 |
| C、Cl2(g)+H2O═2H++ClO-+Cl- K=10-10.9 |
| D、用氯处理饮用水时,pH=7.5时杀菌效果比pH=6.5时差 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com