
Na2FeO4是一种高效多功能水处理剂, 应用前景十分看好。一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,对此反应下列说法中正确的是
应用前景十分看好。一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,对此反应下列说法中正确的是
A.Na2O2只作氧化剂
B.Na2FeO4既是氧化产物又是还原产物
C.O2是还原产物
D.2 mol FeSO4发生反应时,反应中共有8 mol电子转移
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
(1)通过点燃的方法可以鉴别聚乙烯和聚氯乙烯。如果塑料点燃时有强烈的刺激性气味,这种塑料可能是由 制成的。
(2)某同学设计了如图所示实验来验证塑料燃烧的产物。
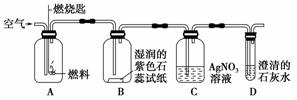
若A瓶燃烧的是聚氯乙烯塑料,在B瓶中可以看到的现象是________________________________________________________________________,
C、D两瓶中发生反应的化学方程式为________________________________________________________________________。
若A瓶中用的是聚乙烯塑料,则在C瓶中 (“能”或“不能”)观察到沉淀。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.5×10-16,Ksp(Ag2CrO4)=2.0×10-12,则下列难溶盐的饱和溶液中,Ag+浓度大小顺序正确的是( )
A.AgCl>AgI>Ag2CrO4 B.AgCl>Ag2CrO4>AgI
C.Ag2CrO4>AgCl>AgI D.Ag2CrO4>AgI>AgCl
查看答案和解析>>
科目:高中化学 来源: 题型:
钡(Ba)和锶(Sr)及其化合物在工业上有着广泛的应用,它们在地壳中常以硫酸盐的形式存在,BaSO4和SrSO4都是难溶性盐。工业上提取钡和锶时首先将BaSO4和SrSO4转化成难溶弱酸盐。
已知:SrSO4(s) Sr2+(aq)+S(aq) Ksp=2.5×10-7
Sr2+(aq)+S(aq) Ksp=2.5×10-7
SrCO3(s) Sr2+(aq)+C
Sr2+(aq)+C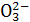 (aq) Ksp=2.5×10-9
(aq) Ksp=2.5×10-9
(1)将SrSO4转化成SrCO3的离子方程式为 ,该反应的平衡常数表达式为 ;该反应能发生的原因是 。
(用沉淀溶解平衡的有关理论解释)
(2)对于上述反应,实验证明增大C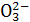 的浓度或降低温度都有利于提高SrSO4的转化率。判断在下列两种情况下,平衡常数K的变化情况(填“增大”“减小”或“不变”):
的浓度或降低温度都有利于提高SrSO4的转化率。判断在下列两种情况下,平衡常数K的变化情况(填“增大”“减小”或“不变”):
①升高温度,平衡常数K将 ;
②增大C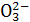 的浓度,平衡常数K将 。
的浓度,平衡常数K将 。
(3)已知,SrSO4和SrCO3在酸中的溶解性与BaSO4和BaCO3类似,设计实验证明上述过程中SrSO4是否完全转化成SrCO3。实验所用的试剂为 ;实验现象及其相应结论为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
某校化学研究性学习小组设计如下实验方案,测定放置已久的小苏打样品中纯碱的质量分数。
(1)方案一:称取一定质量的样品,置于坩埚中加热至恒重后,冷却,称取剩余固体质量,计算。实验中加热至恒重的目的是 。
(2)方案二:按下图装置进行实验。并回答以下问题。
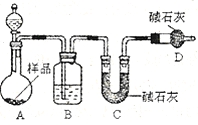
① 实验前先 。分液漏斗中应该装 (“盐酸”或“硫酸”)。D装置的作用是 。
② 实验中除称量样品质量外,还需称 装置前后质量的变化。
③ 根据此实验得到的数据,测定结果有误差。因为实验装置还存在一个明显缺陷,该缺陷是 。
(3)方案三:称取一定量样品,置于小烧杯中,加适量水溶解,向小烧杯中加入足量氯化钡溶液。过滤洗涤,干燥沉淀,称量固体质量,计算:
① 过滤操作中,除了烧杯,漏斗外,还用到的玻璃仪器有 。
② 实验中判断沉淀是否完全的方法是 。
③ 已知称得样品21.2g,干燥的沉淀质量为19.7g,则样品中碳酸钠的质量分数为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,用 0.1000 mol·L
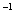 NaOH溶液滴定 20.00mL0.1000 mol·L
NaOH溶液滴定 20.00mL0.1000 mol·L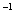
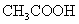 溶液所得滴定曲线如图。下列说法正确的是
溶液所得滴定曲线如图。下列说法正确的是
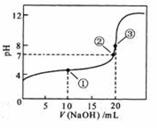
A.点①所示溶液中: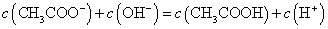
B.点②所示溶液中: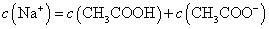
C.点③所示溶液中: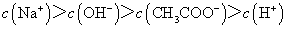
D.滴定过程中可能出现: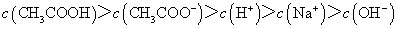
查看答案和解析>>
科目:高中化学 来源: 题型:
设计实验方案是科学探究的重要环节。以下化学实验设计中,能达到实验目的的是( )
A.用铜和稀硫酸反应制取硫酸铜溶液
B.用石灰石除去氯化钙溶液中混有的盐酸
C.用氢氧化钠溶液除去二氧化碳中混有的氯化氢气体
D.用酚酞试液检验暴露在空气中的NaOH固体是否变质
查看答案和解析>>
科目:高中化学 来源: 题型:
在两个恒容的密闭容器中进行下列两个可逆反应:
甲中,C(s)+H2O(g) CO(g)+H2(g)
CO(g)+H2(g)
乙中,CO(g)+H2O(g)  CO2(g)+H2(g)。现有下列状态:①混合气体平均相对分子质量不再改变;②恒温时,气体压强不再改变;③各气体组分浓度相等;
CO2(g)+H2(g)。现有下列状态:①混合气体平均相对分子质量不再改变;②恒温时,气体压强不再改变;③各气体组分浓度相等;
④反应体系中温度保持不变;⑤断裂氢氧键速率等于断裂氢氢键速率的2倍;⑥混合气体密度不变;⑦单位时间内,消耗水的质量与生成氢气的质量之比为9∶1;⑧同一时间内,水蒸气消耗的物质的量等于氢气消耗的物质的量。其中能表明甲、乙容器中反应都达到平衡状态的是( )
A.①②⑤ B.③④⑥ C.⑥⑦⑧ D.④⑤⑧
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com