
【题目】NaBH4容易与H+反应产生氢气而成为储氢材料研究的热点。以硼酸为原料制备NaBH4的一种工艺流程如下图所示:
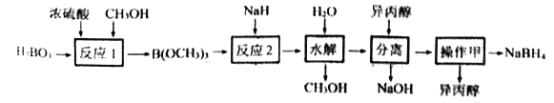
已知: ①H3BO3电离:H3BO3+H2O![]() [B(OH)4]-+H+
[B(OH)4]-+H+
②反应1: H3BO3+3CH3OH![]() B(OCH3)3+3H2O
B(OCH3)3+3H2O
③反应2:B(OCH3)3+4NaH= NaBH4+ 3CH3ONa
(1)H3BO3是____元酸,NaH的电子式为_______________。
(2)NaBH4与水剧烈反应放出H2。反应的化学方程式为________________。
(3)反应1属于______(填有机反应类型),反应过程中蒸出B(OCH3)3的目的是__________。
(4)“水解”时产生的大量NaOH,减缓了NaBH4与水的反应。在该步骤中,与水反应生成大量NaOH的物质是_________。
(5)“分离”后得到NaBH4的异丙醇溶液。操作甲是_____________。
(6)上述流程中可以循环使用的物质是____________。
(7)以惰性电极电解Na[B(OH)4]与NaOH 混合溶液也能制得NaBH4。阴极的电极反应式为___。
【答案】 一 ![]() NaBH4+4H2O=Na[B(OH)4]+4H2↑ 取代(或酯化)反应 降低生成物的浓度,有利于反应1向正反应方向移动 CH3ONa、NaH 蒸馏 CH3OH、异丙醇 [B(OH)4] -+8e-+4H2O=BH4-+8OH-
NaBH4+4H2O=Na[B(OH)4]+4H2↑ 取代(或酯化)反应 降低生成物的浓度,有利于反应1向正反应方向移动 CH3ONa、NaH 蒸馏 CH3OH、异丙醇 [B(OH)4] -+8e-+4H2O=BH4-+8OH-
【解析】考查化学工艺流程,(1)判断某酸属于几元酸,看电离出H+的个数,根据信息①,H3BO3只能电离出一个H+,因此H3BO3属于一元酸;NaH中Na显+1价,H显-1价,NaH属于离子化合物,因此NaH的电子式为![]() ;(2)NaBH4中Na显+1价,B显+3价,H显-1价,H2O的H显+1价,因此发生化学方程式为NaBH4+4H2O=NaB(OH)4+4H2↑;(3)根据信息②,CH3OH属于醇,H3BO3属于含氧酸,因此CH3OH与H3BO3发生取代反应或酯化反应;信息②,反应1属于可逆反应,蒸出B(OCH3)3,降低生成物的浓度,促使反应向正反应方向进行,提高原料的利用;(4)反应2中加入NaH,水解时加入H2O,因此NaH与H2O反应:NaH+H2O=NaOH+H2↑,CH3ONa+H2O=CH3OH+NaOH,因此该步骤中,与水反应生成大量的NaOH的物质是NaH和CH3ONa;(5)NaHB4的异丙醇溶液,它们互为混合,利用其沸点不同,采用蒸馏的方法进行分离;(6)根据流程,循环使用的物质是CH3OH和异丙醇;(7)制备NaBH4,H的化合价降低,在阴极上得到电子,因此阴极反应式为[B(OH)4] -+8e-+4H2O=BH4-+8OH-。
;(2)NaBH4中Na显+1价,B显+3价,H显-1价,H2O的H显+1价,因此发生化学方程式为NaBH4+4H2O=NaB(OH)4+4H2↑;(3)根据信息②,CH3OH属于醇,H3BO3属于含氧酸,因此CH3OH与H3BO3发生取代反应或酯化反应;信息②,反应1属于可逆反应,蒸出B(OCH3)3,降低生成物的浓度,促使反应向正反应方向进行,提高原料的利用;(4)反应2中加入NaH,水解时加入H2O,因此NaH与H2O反应:NaH+H2O=NaOH+H2↑,CH3ONa+H2O=CH3OH+NaOH,因此该步骤中,与水反应生成大量的NaOH的物质是NaH和CH3ONa;(5)NaHB4的异丙醇溶液,它们互为混合,利用其沸点不同,采用蒸馏的方法进行分离;(6)根据流程,循环使用的物质是CH3OH和异丙醇;(7)制备NaBH4,H的化合价降低,在阴极上得到电子,因此阴极反应式为[B(OH)4] -+8e-+4H2O=BH4-+8OH-。


科目:高中化学 来源: 题型:
【题目】下图转化关系中的m、n、p、q均含氯元素的常见物质,其中p、q为酸,n为单质,下列叙述不正确的是( )
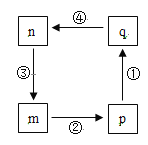
A. n在标况下的密度约为3.17 g·L-1
B. 反应③中物质n与电子转移的物质的量相等
C. p氧化性强于q
D. 四步反应均为氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜的相关化合物在生产生活中具有重要的作用。回答下列问题:
(1)铜元素在周期表中的位置是______________,基态铜原子中,核外电子占据最高能层的符号是_________________,占据该最高能层的电子数为__________________。
(2)在一定条件下,金属相互化合形成的化合物称为金属互化物,如Cu9Al4、Cu5Zn8等。某金属互化物具有自范性,原子在三维空间里呈周期性有序排列,该金属互化物属于__________(填“晶体”或“非晶体”)。
(3)铜能与类卤素[(SCN)2]反应生成Cu(SCN)2,1mol(SCN)2分子中含有σ键的数目为______________。 (SCN)2对应的酸有硫氰酸(H-S-C![]() N)、异硫氰酸(H-N=C=S)两种。理论上前者沸点低于后者,其原因是____________________________。
N)、异硫氰酸(H-N=C=S)两种。理论上前者沸点低于后者,其原因是____________________________。
(4)铜晶体中铜原子的堆积方式为面心立方堆积,每个铜原子周围距离最近的铜原子个数为________。
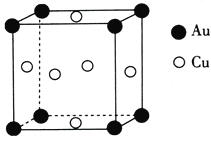
(5)铜与金形成的金属互化物的晶胞结构如图所示,其晶胞边长为a nm,该金属互化物的密度为____________(用含a、NA的代数式表示)g·cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物M为海洋天然产物(一)-PavidolideB不对称全合成的中间体之一,结构简式如下图。下列有关M的说法不正确的是

A. 分子式为C10H14O
B. 可发生取代反应加成反应、聚合反应
C. 分子中所有碳原子都在同一平面上
D. 苯环上连有-OH和-C4H9的M的同分异构体有12种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,甲池的总反应式为:N2H4+O2=N2+H2O,下列关于该电池工作时的说法正确的是( )
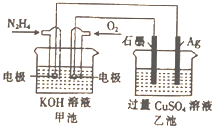
A. 该装置工作时,Ag电极上有气体生成
B. 甲池中负极反应为N2H4-4e-=N2+4H+
C. 甲池和乙池中的溶液的pH均减小
D. 当甲池中消耗0.1molN2H4时,乙池中理论上最多产生6.4g固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数,则下列叙述中正确的是
A. 6.02×1022个H2SO分子在水中可电离生成2NA个H+
B. 在0℃、101kPa时,22.4L氢气中含有NA个氢原子
C. 14g氮气中含有7NA个电子
D. NA个一氧化碳分子和0.5mol甲烷的质量比为7︰4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以异丙苯(A)为原料合成(±)-水芹醛(C10H16O)的路线如下:

(1)(土)-水芹醛的官能团名称为______、_______。
(2)G→H反应的方程式为_____________。
(3)H→I的反应类型为_____________。
(4)B、K的结构简式分别为_____________、_____________。
(5)鉴别J和(土)一水芹醛可选用的试剂为___________。
a.NaHCO3溶液 b.溴水 c.酸性KMnO4溶液 d.新制Cu(OH)2
(6)满足下列条件的D的同分异构体有___种,其中核磁共振氢谱为1:1:2:2:6的结构简式为____。
①能与金属钠反应产生氢气;
②不能使FeCl3溶液显色;
③含有苯环且苯环上不超过两个取代基。
(7)依据题中信息,参照上述路线,以![]() 为原料,选择必要试剂设计
为原料,选择必要试剂设计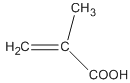 的合成路线____________。
的合成路线____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上通过电化学原理在铝片表面形成氧化膜来提高其抗腐蚀能力,工作原理如下图所示。列说法正确的是
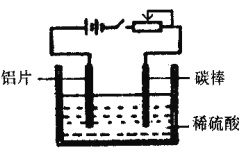
A. 碳棒可用任意金属代替,其作用是传递电流
B. 通电一段时间后,溶液的pH增大
C. 通电后电子被强制从碳棒流向铝片使铝表面形成氧化膜
D. 可通过调节滑动变阻器来控制氧化膜的形成速度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com