
”¾ĢāÄæ”放»Æѧ-Ń”ŠŽ3:ĪļÖŹ½į¹¹ÓėŠŌÖŹ”æĆĢ¼°Ęä»ÆŗĻĪļÓĆĶ¾·Ē³£¹ć·ŗ”£»Ų“šĻĀĮŠĪŹĢā:
(1)Al70Pd21Mn9ŹĒŅ»ÖÖ×¼¾§Ģå(½éÓŚ¾§ĢåŗĶ·Ē¾§ĢåÖ®¼äµÄ¹ĢĢå),ÄÜ×¼Č·Ö¤Ć÷Ęä²»ŹĒ¾§ĢåµÄ·½·ØŹĒ___________”£
(2)»łĢ¬MnŌ×ӵļŪµē×ÓÅŲ¼Ź½ĪŖ_________,Ī“³É¶Ōµē×ÓŹżĪŖ_____øö”£
(3)MnSČŪµć(1610”ę)±ČMnOČŪµć(1650”ę)µĶ,ĘäŌŅņŹĒ____________”£
(4)ĆĢµÄŅ»ÖÖÅäŗĻĪļµÄ»ÆѧŹ½ĪŖ[Mn(CO)5(CH3CN)]Br”£
¢ŁÅäŗĻĪļÖŠĆĢŌŖĖŲµÄ¼ŪĢ¬ĪŖ________”£
¢ŚÅäĢåCH3CNÓėÖŠŠÄŌ×ÓŠĪ³ÉÅäĪ»¼üŹ±,Ģį¹©¹Ā¶Ōµē×ÓµÄŌ×ÓŹĒ_____,øĆ·Ö×ÓÖŠĢ¼Ō×ÓµÄŌӻƷ½Ź½ĪŖ_______£»C”¢H”¢NµÄµēøŗŠŌ“ӓ󵽊”µÄĖ³ŠņĪŖ________”£
(5)ĆĢµÄŗ¬ŃõĖįÓŠHMnO4(øßĆĢĖį)”¢H2MnO3(ŃĒĆĢĖį),øßĆĢĖįµÄĖįŠŌ±ČŃĒĆĢĖįĒæ,ĄķÓÉŹĒ_________”£
(6)ijÖÖŗ¬ĆĢĢŲŹā²ÄĮĻµÄ¾§°ū½į¹¹ČēĻĀĶ¼ĖłŹ¾:
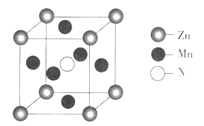
Čō¾§°ū²ĪŹżĪŖanm,ÓĆNA±ķŹ¾°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ,ŌņøĆ¾§°ūµÄĆܶČĪŖ____(ĮŠ³ö“śŹżŹ½¼“æÉ)”£
”¾“š°ø”æ XÉäĻßŃÜÉ䏵Ńé 3d54s2 5 S2-µÄ°ė¾¶±ČO2-µÄ“ó£¬MnSµÄ¾§øńÄÜŠ” +1 N(µŖ) spŗĶsp3 N>C>H øßĆĢĖį·Ö×Ó(HOMnO3)ÖŠŗ¬ÓŠČżøö·ĒōĒ»łŃõŌ×Ó£¬ŃĒĆĢĖį[(HO)2MnO]ÖŠÖ»ÓŠŅ»øö·ĒōĒ»łŃõŌ×Ó ![]() g/cm3
g/cm3
”¾½āĪö”æ(1)¾§Ģå¾ßÓŠĪ¢¹ŪµćÕó½į¹¹£¬ÄÜ·¢ÉśXÉäĻßŃÜÉäĻÖĻ󣬹ŹÄÜ×¼Č·Ö¤Ć÷Al70Pd21Mn9²»ŹĒ¾§ĢåµÄ·½·ØŹĒXÉäĻßŃÜÉ䏵Ń飬Čō²»²śÉśXÉäĻßŃÜÉäĻÖĻó£¬Ōņ²»ŹĒ¾§Ģ唣±¾Ģā“š°øĪŖ£ŗXÉäĻßŃÜÉ䏵Ń锣
(2)MnŹĒ25ŗÅŌŖĖŲ¼Ūµē×ÓÅŲ¼Ź½ĪŖ3d54s2,5øö3dµē×Ó·Ö±šĪ»ÓŚ5øö²»Ķ¬µÄ¹ģµĄÉĻ£¬ÓŠ5øöĪ“³É¶Ōµē×Ó”£
(3) MnSŗĶMnO¾§ĢåĄąŠĶĻąĶ¬£¬ÓÉÓŚS2-µÄ°ė¾¶±ČO2-µÄ“ó£¬ŌņMnSµÄ¾§øńÄܱČMnOŠ”£¬MnSČŪµć±ČMnOČŪµćµĶ”£¹Ź±¾Ģā“š°øĪŖ£ŗS2-µÄ°ė¾¶±ČO2-µÄ“ó£¬MnSµÄ¾§øńÄÜŠ””£
(4) ¢ŁÅäŗĻĪļ[Mn(CO)5(CH3CN)]BrµÄÅäĢåÓŠCO”¢CH3CN·Ö×ÓŗĶBr-,øł¾Ż»ÆŗĻ¼Ū“śŹżŗĶĪŖĮć£¬ÅäŗĻĪļÖŠĆĢŌŖĖŲµÄ¼ŪĢ¬ĪŖ+1£»
¢ŚÅäĢåCH3CNÓėÖŠŠÄŌ×ÓŠĪ³ÉÅäĪ»¼üŹ±,Ģ¼Ō×Ó¼Ūµē×Ó¶¼ÓĆÓŚŠĪ³É¹²ÓƵē×Ó¶Ō£¬µŖŌ×Ó5øö¼Ūµē×ÓÓŠČżøöŠĪ³É¹²ÓƵē×Ó¶Ō£¬»¹ÓŠŅ»¶Ō¹Ā¶Ōµē×Ó£¬ĖłŅŌĢį¹©¹Ā¶Ōµē×ÓµÄŌ×ÓŹĒµŖŌ×Ó,øĆ·Ö×ÓÖŠĮ½øöĢ¼Ō×ÓĘäÖŠCH3-ÉĻĢ¼Ō×ÓµÄŌӻƷ½Ź½ĪŖsp3 £¬-CNÉĻµÄĢ¼Ō×ÓŌӻƷ½Ź½ĪŖsp£»ŌŖĖŲµÄ·Ē½šŹōŠŌŌ½Ē棬ĪüŅżµē×ÓÄÜĮ¦Ō½Ē棬ŌņµēøŗŠŌŌ½“ó£¬ĖłŅŌC”¢H”¢NµÄµēøŗŠŌ“ӓ󵽊”µÄĖ³ŠņĪŖN>C>H£»¹Ź±¾Ģā“š°øĪŖ£ŗ+1 £»N(µŖ) £» spŗĶsp3 £»N>C>H£»
(5)HMnO4ŗĶH2MnO3¶¼ŹĒŗ¬ŃõĖį,øßĆĢĖįŹĒŅ»ŌŖĖį£¬ŗ¬ÓŠČżøö·ĒōĒ»łŃõ£¬ŃĒĆĢĖįĪŖ¶žŌŖĖį£¬ŗ¬ÓŠŅ»øö·ĒōĒ»łŃõ,ŗ¬ōĒ»łŃõŌ½¶ąĖįŠŌŌ½Ē棬ĖłŅŌøßĆĢĖįµÄĖįŠŌ±ČŃĒĆĢĖįĒ棻¹Ź±¾Ģā“š°øĪŖ£ŗ
øßĆĢĖį·Ö×Ó(HOMnO3)ÖŠŗ¬ÓŠČżøö·ĒōĒ»łŃõŌ×Ó£¬ŃĒĆĢĖį[(HO)2MnO]ÖŠÖ»ÓŠŅ»øö·ĒōĒ»łŃõŌ×Ó”£
(6) øł¾Ż¾§°ū½į¹¹¼ĘĖćŗ¬ÓŠµÄŌ×ÓŹż£¬ŗ¬ÓŠZnŌ×ÓŹż: 8![]() =1,ŗ¬MnŌ×ÓŹż6
=1,ŗ¬MnŌ×ÓŹż6![]() =3£¬ŗ¬ÓŠNŌ×ÓŹż£ŗ1øö£¬¹Ź¾§°ūÖŠZn”¢Mn”¢NŌ×ÓøöŹż±ČĪŖ1:3:1£¬ZnMn3NµÄĦ¶ūÖŹĮæŹĒ244g/mol,£¬¾Żm=
=3£¬ŗ¬ÓŠNŌ×ÓŹż£ŗ1øö£¬¹Ź¾§°ūÖŠZn”¢Mn”¢NŌ×ÓøöŹż±ČĪŖ1:3:1£¬ZnMn3NµÄĦ¶ūÖŹĮæŹĒ244g/mol,£¬¾Żm=![]() VµĆ£ŗ
VµĆ£ŗ![]() 10-7£©3 cm3NA/mol=244g/mol£¬
10-7£©3 cm3NA/mol=244g/mol£¬![]()
![]() g/cm3£¬¹Ź±¾Ģā“š°øĪŖ£ŗ
g/cm3£¬¹Ź±¾Ģā“š°øĪŖ£ŗ![]() g/cm3”£
g/cm3ӣ



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ25”ꏱ£¬¼øÖÖČõĖįµÄµēĄėĘ½ŗā³£ŹżČēĻĀ±ķĖłŹ¾£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
»ÆѧŹ½ | HCOOH | H2CO3 | HCN |
µēĄėĘ½ŗā³£Źż | K=1.8”Į10-4 | K1=4.3”Į10-7 K2=5.6”Į10-11 | K=4.9”Į10-10 |
A. H2CO3ČÜŅŗŗĶNaCNČÜŅŗ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖH2CO3+CN-==HCO3-+HCN
B. HCOOHµÄµēĄėĘ½ŗā³£Źż±ķ“ļŹ½ĪŖK= c(HCOOH)/[c(HCOO-)”¤c(H+)]
C. Na2CO3ČÜŅŗĻŌ¼īŠŌ£¬NaHCO3ČÜŅŗĻŌĖįŠŌ
D. ĖįŠŌĒæČõĖ³ŠņŹĒHCOOH>HCN>H2CO3
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÉčNA±ķŹ¾°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ£¬ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ
A. ±ź×¼×“æöĻĀ£¬22.4L ŗ¤ĘųÓė 1molĒāĘųĖłŗ¬Ō×ÓŹż¾łĪŖ 2NA
B. 25 ”ę”¢1.01”Į105PaŹ±£¬2.24 L Cl2ÖŠŗ¬ÓŠµÄŌ×ÓŹżĪŖ0.2”Į6.02”Į1023
C. ³£ĪĀ³£Ń¹ĻĀ£¬S2ŗĶS8µÄ»ģŗĻĪļ¹²6.4 g£¬Ėłŗ¬ĮņŌ×ÓŹżŅ»¶ØĪŖ0.2 NA
D. ½«100 mL 0.1 molL©1µÄFeCl3ČÜŅŗµĪČė·ŠĖ®ÖŠæÉÖʵĆFe(OH)3½ŗĮ£ŹżÄæĪŖ0.01 NA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ³£ĪĀĻĀ,ÓƵČÅØ¶ČµÄNaOHČÜŅŗ·ÖeµĪ¶ØĻąĶ¬Ģå»żµÄNH4Cl”¢KH2PO4¼°CH3COOHČÜŅŗ£¬µĪ¶ØĒśĻßČēĻĀĶ¼ĖłŹ¾:
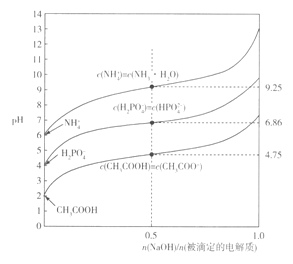
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A. NH3”¤H2O===NH4++OH-µÄlg K =-9.25
B. 0.1mol/LKH2PO4ČÜŅŗÖŠ:c( HPO42- )<c(H3PO4)
C. CH3COOH+HPO42-=CH3COO-+H2PO4-µÄlg K = -11.61
D. ŌŚµĪ¶Ø¹ż³ĢÖŠ£¬µ±ČÜŅŗpHĻąĶ¬Ź±,ĻūŗÄNaOH µÄĪļÖŹµÄĮæ:CH3COOH>KH2PO4> NH4Cl
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ£Ø1£©“æ¾»ĪļæÉøł¾ŻĘä×é³ÉŗĶŠŌÖŹ½ųŠŠ·ÖĄą”£ČēĶ¼ĖłŹ¾µÄ·ÖĄą·½·ØŹōÓŚ________(Ģī×ÖÄø)”£

A£®½»²ę·ÖĄą·Ø
B£®Ź÷ד·ÖĄą·Ø
£Ø2£©ČĖĆĒŅŌ_________________________________ĪŖ·ÖĄą±ź×¼·Ö³öČÜŅŗ”¢½ŗĢåŗĶ×ĒŅŗČżÖÖĢåĻµ£¬ĒėŠ“³öŹµŃéŹŅÖʱøFe(OH)3½ŗĢåµÄ»Æѧ·½³ĢŹ½£ŗ______________________________;
£Ø3£©ŅŌH”¢O”¢S”¢N¼øÖÖŌŖĖŲÖŠČĪŅāĮ½ÖÖ»ņČżÖÖŌŖĖŲ×é³ÉŗĻŹŹµÄ³£¼ūĪļÖŹ£¬·Ö±š½«ĘäÖŠŅ»ÖÖ³£¼ūĪļÖŹµÄ»ÆѧŹ½ĢīŌŚĻĀ±ķĻąÓ¦Ąą±šÖŠ£ŗ
ĪļÖŹĄą±š | ·Ēŗ¬ŃõĖį | ¼ī | ĖįŹ½ŃĪ | ĖįŠŌŃõ»ÆĪļ |
»ÆѧŹ½ | ____________ | ___________ | ___________ | __________ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĖµ·ØÖŠ£¬ÕżČ·µÄŅ»ĻīŹĒ£Ø””””£©
A.ŅņĪŖCuæÉŅŌµ¼µē£¬ĖłŅŌCuŹĒµē½āÖŹ
B.ŅņĪŖNaHSO4æÉŅŌµēĄė³öH+ £¬ ĖłŅŌŹōÓŚĖį
C.ĪäµĀŗĻ½šČŪµćµĶ£Ø70”ę£©£¬æÉŅŌ×ö±£ĻÕĖæ
D.Ōģ³ÉĖįÓźµÄÖ÷ŅŖ“óĘųĪŪČ¾ĪļŹĒSO2ŗĶCO2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”潫100 mL 2 mol/L AlCl3ČÜŅŗøśŅ»¶ØĢå»ż4 mol/L NaOHČÜŅŗ»ģŗĻŗóæɵĆ7.8 g³Įµķ£¬ŌņNaOHČÜŅŗµÄĢå»żæÉÄÜŹĒ£ŗ¢Ł75 mL ¢Ś150 mL ¢Ū175 mL ¢Ü200 mL
A. ¢Ł B. ¢Ś C. ¢Ł¢Ū D. ¢Ś¢Ū
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æI£®ŅŃÖŖ2KMnO4£«5H2C2O4£«3H2SO4===K2SO4£«2MnSO4£«8H2O£«10CO2”ü£¬ŌŚæŖŹ¼Ņ»¶ĪŹ±¼äÄŚ£¬·“Ó¦ĖŁĀŹ½ĻĀż£¬ČÜŅŗĶŹÉ«²»Ć÷ĻŌ£»µ«²»¾ĆĶ»Č»ĶŹÉ«£¬·“Ó¦ĖŁĀŹĆ÷ĻŌ¼Óæģ”£
£Ø1£©Õė¶ŌÉĻŹöĻÖĻó£¬Ä³Ķ¬Ń§ČĻĪŖøĆ·“Ó¦·ÅČČ£¬µ¼ÖĀČÜŅŗĪĀ¶ČÉĻÉż£¬·“Ó¦ĖŁĀŹ¼Óæģ”£“ÓÓ°Ļģ»Æѧ·“Ó¦ĖŁĀŹµÄŅņĖŲæ“£¬Äć²ĀĻė»¹æÉÄÜŹĒ__________________µÄÓ°Ļģ”£
£Ø2£©ČōÓĆŹµŃéÖ¤Ć÷ÄćµÄ²ĀĻė£¬³żĖįŠŌøßĆĢĖį¼ŲČÜŅŗ”¢²ŻĖįČÜŅŗĶā£¬æÉŅŌŌŚ·“Ó¦Ņ»æŖŹ¼Ź±¼ÓČė__________________”£
A£®ĮņĖį¼Ų B£®ĮņĖįĆĢ C£®ĀČ»Æ¼Ų D£®Ė®
II. ·Ö±šČ”40mLµÄ0.50mol/LŃĪĖįÓė40mL 0.55mol/LĒāŃõ»ÆÄĘČÜŅŗ½ųŠŠÖŠŗĶ·“Ó¦”£Ķعż²ā¶Ø·“Ó¦¹ż³ĢÖŠĖł·Å³öµÄČČĮææɼĘĖćÖŠŗĶČČ”£Ēė»Ų“šĻĀĮŠĪŹĢā”£
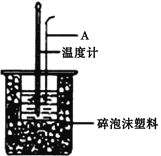
£Ø1£©ŅĒĘ÷AµÄĆū³ĘŹĒ__________________£¬ÉÕ±¼äĢīĀśĖéÅŻÄĖÜĮĻµÄ×÷ÓĆŹĒ__________________”£
£Ø2£©¼ÓČėNaOHČÜŅŗµÄÕżČ·²Ł×÷ŹĒ__________________ (Ģī×ÖÄø£©”£
A£®ŃŲ²£Į§°ō»ŗĀż¼ÓČė B£®Ņ»“ĪŃøĖŁ¼ÓČė C£®·ÖČż“Ī¼ÓČė
£Ø3£©¼ŁÉčŃĪĖįŗĶĒāŃõ»ÆÄĘČÜŅŗµÄĆܶȶ¼ŹĒ1g/cm3£¬ÓÖÖŖÖŠŗĶŗóÉś³ÉČÜŅŗµÄ±ČČČČŻc£½4.18J/£Øg”¤”ę£©”£ĪŖĮĖ¼ĘĖćÖŠŗĶČČ£¬Ä³Ń§ÉśŹµŃé¼ĒĀ¼Źż¾ŻČēĻĀ£ŗ
ŹµŃéŠņŗÅ | ĘšŹ¼ĪĀ¶Čt1”ę | ÖÕÖ¹ĪĀ¶Čt2”ę | |
ŃĪĖį | ĒāŃõ»ÆÄĘ | »ģŗĻČÜŅŗ | |
1 | 20.0 | 20.1 | 23.2 |
2 | 20.2 | 20.4 | 23.4 |
3 | 20.5 | 20.6 | 23.6 |
ŅĄ¾ŻøĆѧɜµÄŹµŃ鏿¾Ż¼ĘĖć£¬øĆŹµŃé²āµĆµÄÖŠŗĶČČ”÷H£½__________________£Ø½į¹ū±£ĮōŅ»Ī»Š”Źż£©”£
£Ø4£©ŹµŃéÖŠČōøÄÓĆ50 mL 0.50 mol/LµÄŃĪĖįÓė40 mL 0.55 mol/LµÄĒāŃõ»ÆÄĘČÜŅŗ½ųŠŠ·“Ó¦£¬ ÓėÉĻŹöŹµŃéĻą±Č£¬Ėł·Å³öµÄČČĮæ__________________(Ģī”°ĻąµČ”±”°²»ĻąµČ”±)£¬ČōŹµŃé²Ł×÷¾łÕżČ·£¬ŌņĖłĒóÖŠŗĶČČ__________________(Ģī”°ĻąµČ”±”°²»ĻąµČ”±)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ·“Ó¦²»ŹōÓŚČ”“ś·“Ó¦µÄŹĒ
A. ŅŅĶéÓėĀČĘų·“Ó¦ B. ŅŅĻ©ÓėäåĖ®µÄ·“Ó¦
C. ±½µÄĻõ»Æ·“Ó¦ D. ±½ÓėŅŗäåµÄ·“Ó¦
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com