
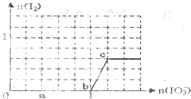
 已知:还原性还原性HSO3->I-,氧化性IO3->I2.在含3mol NaHSO3的溶液中逐滴加入KIO3溶液.加入KIO3和析出I2的物质的量的关系曲线如图所示.下列说法正确的是( )
已知:还原性还原性HSO3->I-,氧化性IO3->I2.在含3mol NaHSO3的溶液中逐滴加入KIO3溶液.加入KIO3和析出I2的物质的量的关系曲线如图所示.下列说法正确的是( )| A、反应过程中的氧化产物均为SO3 |
| B、a点时剩余NaHSO3的物质的量为1.2 mol |
| C、b点时的还原产物可能是KI或NaI |
| D、当溶液中I-与I2的物质的量之比为1:1时,加入的KIO3为1.1mol |
| 0.4mol |
| 1 |
| n |
| 3 |
| 5n |
| 3 |
| 5n |
| 3 |
| 5n |
| 3 |
| 3 |
| 8 |
| n |
| 3 |
| 1 |
| 8 |
| 9 |
| 8 |


科目:高中化学 来源: 题型:
| A、CN-中碳元素的化合价为+2 |
| B、该反应的产物之一是无毒的N2 |
| C、当1 mol CN-参与反应时,转移3 mol e- |
| D、处理含0.1 mol CN-的废水,理论上需要消耗标准状况下Cl2的体积为5.6 L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、利用化学平衡常数判断化学反应进行的快慢 |
| B、利用溶解度数据判断氧化还原反应发生的可能性 |
| C、利用沸点数据推测将一些液体混合物分离的可能性 |
| D、利用物质的摩尔质量判断相同状态下不同物质密度的大小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
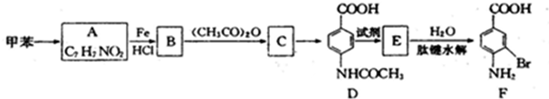
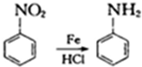
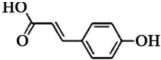
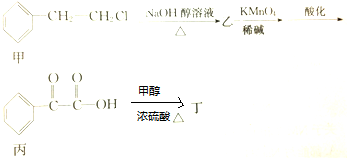
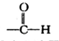 ②苯环上有两个取代基,且处于对位
②苯环上有两个取代基,且处于对位查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、发生析氢腐蚀 |
| B、铁粉作阴极发生氧化反应 |
| C、含有1.12g铁粉的脱氧剂,理论上最多能吸收氧气336mL(标准状况) |
| D、可以吸热,从而降低温度,起保鲜糕点的作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
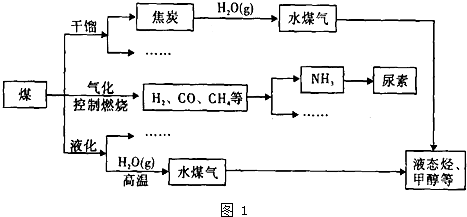
| 化学键 | C-H | H-O | H-H | C-O | C=O |
| 键能/KJ mol-1 | 413 | 463 | 436 | 358 | 802 |
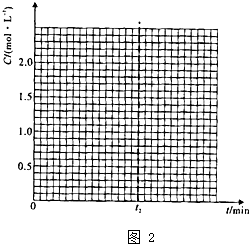 CO中的C与O之间为叁键连接,则CO中碳氧叁键的键能是
CO中的C与O之间为叁键连接,则CO中碳氧叁键的键能是| CH3OH(g) | CH3OCH3(g) | H2O(g) | |
| 起始浓度/mol?L-1 | 2.00 | 0.50 | 0 |
| 平衡浓度/mol?L-1 | c1 | 1.00 | c2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
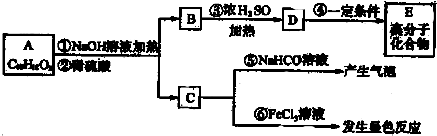
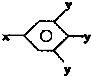 (其中-x、一y均为官能团).请回答下列问题:
(其中-x、一y均为官能团).请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com