
【题目】工业上消除氮氧化物的污染,可用如下反应:![]()
![]() 在温度
在温度![]() 和
和![]() 时,分别将
时,分别将![]() 和
和![]() 充入体积为1L的密闭容器中,测得
充入体积为1L的密闭容器中,测得![]() 随时间变化数据如下表:下列说法错误的是( )
随时间变化数据如下表:下列说法错误的是( )
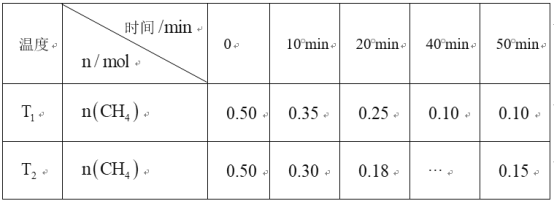
A.10min内,![]() 时
时![]() 的化学反应速率比
的化学反应速率比![]() 时小
时小
B.温度:![]()
C.![]()
D.平衡常数:![]()
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:
【题目】某温度下:![]() 。取适量黄色
。取适量黄色![]() 固体配制成100mL溶液,配制过程中溶液的离子浓度与时间的变化关系如图所示。下列说法中正确的是( )
固体配制成100mL溶液,配制过程中溶液的离子浓度与时间的变化关系如图所示。下列说法中正确的是( )
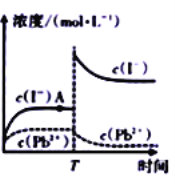
A. A点处可表示![]() 的不饱和溶液
的不饱和溶液
B. T时刻有可能向该![]() 溶液中加人了KI 固体
溶液中加人了KI 固体
C. 常温下![]() 饱和溶液中的
饱和溶液中的![]()
D. 向A点处的![]() 悬浊液中加入
悬浊液中加入![]() 的
的![]() 溶液,平衡后溶液中的c(Pb2+)<4
溶液,平衡后溶液中的c(Pb2+)<4![]() 10-3mol/L
10-3mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z是三种常见的短周期元素,可以形成XY2、Z2Y、XY3、Z2Y2、Z2X等化合物。已知Y的离子和Z的离子具有相同的电子层结构,X离子比Y离子多1个电子层。
(1)X离子的结构示意图为______。
(2)Z2Y对应水化物的碱性比LiOH的_____(填“强”或“弱”),Z2Y对应水化物的电子式为________________
(3)Z2X属于_____(填“共价”或“离子”)化合物,用电子式表示Z2X的形成过程________________
(4)Z2Y2含有_____键和______键,电子式为___________________,Z2Y2溶于水时发生反应的化学方程式是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验事实:
(1)X+Y2+=X2++Y;(2)Z+2H2O![]() Z(OH)2+H2↑;(3)Z2+离子的放电能力比X2+弱;(4)由Y、W 作电极组成的原电池反应为:Y-2e-=Y2+,由此可知,X、Y、Z、W的还原性由强到弱的顺序是
Z(OH)2+H2↑;(3)Z2+离子的放电能力比X2+弱;(4)由Y、W 作电极组成的原电池反应为:Y-2e-=Y2+,由此可知,X、Y、Z、W的还原性由强到弱的顺序是
A. X > Y > Z > WB. Y > X > W > Z
C. Z > X > Y > WD. Z > Y > X > W
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】部分短周期元素原子半径的相对大小、最高正价或最低负价随原子序数的变化关系如图:
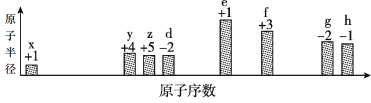
下列说法不正确的是
A.x、z、d三种元素能形成具有强氧化性的酸
B.g、h氧化物对应的水化物都是强酸
C.e最高价氧化物对应的水化物是强碱
D.f的氧化物是两性氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】联合国宣布2019年为“国际化学元素周期表年”。短周期主族元素A、B、C、D、E的原子序数依次增大。A原子的最外层电子数是其内层电子数的2倍,B的单质是空气的最主要成分,C的单质在某些浓酸溶液中能发生钝化,D和A在同一主族,E的其中一种氧化物是造成酸雨的主要物质之一。请回答下列问题:
(1)A元素的名称为_________;元素E在周期表中的位置是________。
(2)A、B、D的原子半径的大小顺序是_________(用元素符号表示)。A和D的简单气态氢化物中稳定性较强的是___________(用化学式表示)。
(3)B和D最高价氧化物对应的水化物中,酸性较强的是___________。若用如图中装置验证这两种酸的酸性强弱,则在装置Ⅱ中加入的试剂分别为__________,观察到的实验现象是__________。
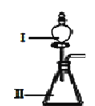
(4)AE2常温下呈液态,则AE2的化学键类型是_______。已知AE2在氧气中完全燃烧,生成AO2和EO2,若 0.1 mol AE2在 1 mol O2中完全燃烧,所得混合气体在标准状况下的体积为________L。
(5)B的最高价氧化物对应的水化物的稀溶液与SO2反应的离子方程式为________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可用于电动汽车的铝—空气燃料电池,通常以NaCl溶液或NaOH溶液为电解液,铝合金为负极,空气电极为正极。下列说法正确的是( )
A.以NaCl溶液或NaOH溶液为电解液时,正极反应都为:O2+2H2O+4e-=4OH-
B.以NaOH溶液为电解液时,负极反应为:Al+3OH--3e-=Al(OH)3↓
C.以NaOH溶液为电解液时,电池在工作过程中电解液的pH保持不变
D.电池工作时,电子通过外电路由正极流向负极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将一定量的气体通入体积为2L的密闭容器中,使其发生反应,,有关物质X、Y、Z的物质的量的变化如图所示。则下列有关推断正确的是( )

A. 该反应的化学方程式为: 3Z = 3X+2Y
B. t0时,X、Y、Z的质量不再改变
C. t0时,Z的浓度为1.2 mol/L
D. t0时,反应停止,反应速率为0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为研究生铁(含碳)与浓硫酸的反应情况及产物性质,设计如下实验。请回答下列问题:

(1)按上图所示装置进行实验(夹持装置及尾气处理装置未画出)。仪器b的名称为___;实验过程中,装置B中观察到的现象是______;装置C中有白色沉淀生成,该沉淀是_____(填化学式)。
(2)装置A中还会产生CO2气体,请写出产生CO2的化学方程式:______。
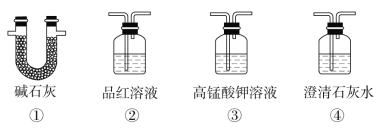
(3)为了验证装置A中产生的气体中含有CO2,应先从下列①~④中选出必要的装置连接A装置中c处管口,从左到右的顺序为____(填序号);然后再进行的操作是从a处多次鼓入N2,其目的是___。
(4)某同学发现实验后期装置A中产生的气体中还含有H2,理由是___________ (用离子方程式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com