
 CH3COO-+H+,对于该平衡,下列叙述正确的是
CH3COO-+H+,对于该平衡,下列叙述正确的是| A.加入水时,平衡向生成CH3COOH的方向移动 |
| B.加入少量NaOH固体,平衡向电离的方向移动 |
| C.加入少量0.1mol·L-1HCl溶液,溶液中c(H+)减小 |
| D.加入少量CH3COONa固体,平衡向电离的方向移动 |
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源:不详 题型:单选题
 Cl2(aq) K1=10-1.2
Cl2(aq) K1=10-1.2 HClO + H+ +Cl- K2=10-3.4
HClO + H+ +Cl- K2=10-3.4 H+ + ClO- Ka=?
H+ + ClO- Ka=?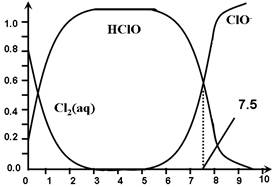
A.Cl2(g)+ H2O  2H+ + ClO- + Cl- K=10-10.9 2H+ + ClO- + Cl- K=10-10.9 |
| B.在氯处理水体系中,c(HClO) + c(ClO-) =c(H+)-c(OH-) |
| C.用氯处理饮用水时,pH=7.5时杀菌效果比pH=6.5时差 |
| D.氯处理饮用水时,在夏季的杀菌效果比在冬季好 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
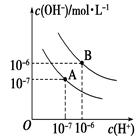
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
 L-1H2SO4洗涤Fe粉,主要反应的化学方程式为 ,之后用蒸馏水洗涤铁粉至中性;
L-1H2SO4洗涤Fe粉,主要反应的化学方程式为 ,之后用蒸馏水洗涤铁粉至中性;查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.NaHS在水中的电离方程式为:NaHS=Na++HS- 和HS-  H++S2- H++S2- |
| B.同物质的量浓度的氨水和盐酸反应至中性时所用体积:V(NH3·H2O)<V(HCl) |
| C.Na2SO3溶液中:c(H+)+ c(HSO3-)+ 2c(H2SO3)= c(OH-) |
| D.同浓度的下列溶液中,c(CH3COO-)的大小:CH3COONa>CH3COONH4>CH3COOH |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.溶液中粒子的数目减小 |
| B.再加入CH3COONa固体能促进醋酸的电离 |
| C.醋酸的电离程度增大,c(H+)亦增大 |
D.溶液中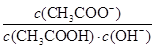 不变 不变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com