
【题目】由乙烯、甲醇等为原料合成有机物G的路线如下:
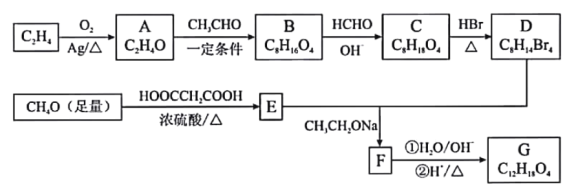
已知:①A分子中只有一种氢;B分子中有四种氢,且能发生银镜反应
②2HCHO+OH-→ CH3OH+HCOO-
③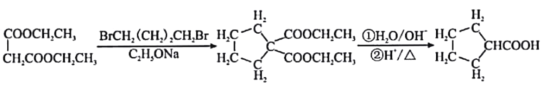
请回答下列问题:
(1)E的化学名称是__________________。
(2)F所含官能团的名称是___________________。
(3)A→B、C→D的反应类型分别是__________________、__________________。
(4)写出B→C的化学方程式__________________。
(5)G的结构简式为__________________。
(6)H是G的同分异构体,写出满足下列条件的H的结构简式__________________。
①1mol H与NaOH溶液反应可以消耗4molNaOH;
②H的核磁共振氢谱有四组峰,峰面积之比为6:1:1:1。
(7)由甲基苯乙醛和X经如图步骤可合成高聚酯L。
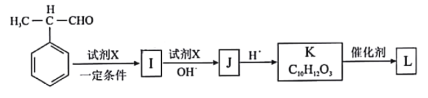
试剂X为________________;L的结构简式为________________________________。
【答案】丙二酸二甲酯 酯基 加成反应 取代反应 

 HCHO
HCHO 
【解析】
A分子中只有一种氢原子,则乙烯与氧气在银作催化剂加热的条件下反应生成环氧乙烷![]() ,A为
,A为![]() ,A与乙醛发生反应生成B,已知B分子中有四种氢,且能发生银镜反应,说明含有醛基,再结合B的分子式C8H16O4,可知B为
,A与乙醛发生反应生成B,已知B分子中有四种氢,且能发生银镜反应,说明含有醛基,再结合B的分子式C8H16O4,可知B为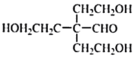 ,根据已知反应②可知,B与甲醛在碱性条件下反应生成C为
,根据已知反应②可知,B与甲醛在碱性条件下反应生成C为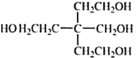 ,C与HBr发生取代反应生成D为
,C与HBr发生取代反应生成D为![]() ,甲醇与丙二酸发生酯化反应生成E为CH3OOCCH2COOCH3,根据已知反应③可知,D与E反应生成F为
,甲醇与丙二酸发生酯化反应生成E为CH3OOCCH2COOCH3,根据已知反应③可知,D与E反应生成F为![]() ,G为
,G为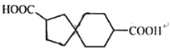 ,据此分析解答。
,据此分析解答。
(1)甲醇与丙二酸发生酯化反应生成E为CH3OOCCH2COOCH3,E的化学名称是丙二酸二甲酯,故答案为:丙二酸二甲酯;
(2)由以上分析知,F为![]() ,则其所含官能团是酯基,故答案为:酯基;
,则其所含官能团是酯基,故答案为:酯基;
(3)A为![]() ,A与乙醛发生反应生成B,已知B分子中有四种氢,且能发生银镜反应,说明含有醛基,再结合B的分子式C8H16O4,可知B为
,A与乙醛发生反应生成B,已知B分子中有四种氢,且能发生银镜反应,说明含有醛基,再结合B的分子式C8H16O4,可知B为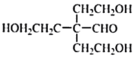 ,则A→B的反应类型是加成反应,C为
,则A→B的反应类型是加成反应,C为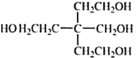 ,C与HBr发生取代反应生成D为
,C与HBr发生取代反应生成D为![]() ,C→D的反应类型是取代反应,故答案为:加成反应;取代反应;
,C→D的反应类型是取代反应,故答案为:加成反应;取代反应;
(4)根据已知反应②可知,B与甲醛在碱性条件下反应生成C为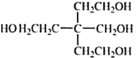 ,反应的化学方程式是
,反应的化学方程式是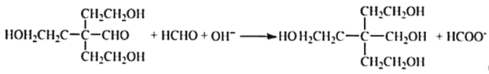 ;
;
(5)由以上分析知,G的结构简式为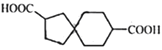 ;
;
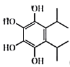
(6)H的分子式为C12H18O4,其不饱和度为![]() ,满足下列条件的H,①1mol H与NaOH溶液反应可以消耗4molNaOH,则其含有苯环,为芳香族化合物,且含有4个酚羟基,②H的核磁共振氢谱有四组峰,峰面积之比为6:1:1:1,则其含有4种等效氢,且氢原子数分别为12、2、2、2,则符合要求的结构简式为
,满足下列条件的H,①1mol H与NaOH溶液反应可以消耗4molNaOH,则其含有苯环,为芳香族化合物,且含有4个酚羟基,②H的核磁共振氢谱有四组峰,峰面积之比为6:1:1:1,则其含有4种等效氢,且氢原子数分别为12、2、2、2,则符合要求的结构简式为 ,故答案为:
,故答案为: ;
;
(7)L为高聚酯,则K中应同时含有羟基和羧基,K中含有10个碳原子, 只有9个碳原子,根据已知反应②可知,
只有9个碳原子,根据已知反应②可知, 与HCHO在一定条件下发生取代反应生成I为
与HCHO在一定条件下发生取代反应生成I为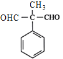 ,I发生已知反应②生成J为
,I发生已知反应②生成J为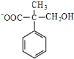 ,J经酸化得到K为
,J经酸化得到K为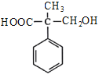 ,K发生缩聚反应生成
,K发生缩聚反应生成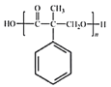 ,故答案为:HCHO;
,故答案为:HCHO; 。
。


科目:高中化学 来源: 题型:
【题目】NO很容易与许多分子迅速发生反应,科学家发现在生物体中不断地产生NO,用于细胞间传递信息;NO还参与心血管系统、免疫系统以及中枢和外围神经系统的调控。
(1)实验室用金属铜和稀硝酸制取NO的离子方程式为:__________________。
(2)NO是有毒气体,某学生为防止污染,用分液漏斗和烧杯装配了一套简易的、能随开随用、随关随停的NO气体发生装置,如图甲所示。
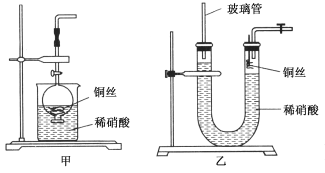
①实验室若没有铜丝,而只有小铜粒,在使用上述装置进行实验时,可用丝状材料包裹铜粒以代替铜丝进行实验,这种丝状材料的成分可以是________(填选项编号)。
A.铁B.铝C.铂D.玻璃
②打开分液漏斗的活塞使反应进行,在分液漏斗中实际看到的气体是红棕色的,原因是____________________(填化学方程式)。
(3)为证明铜丝与稀硝酸反应生成的确实是NO,某学生另设计了一套如图乙所示的装置制取NO。反应开始后,可以在U形管右端观察到无色的NO气体。长玻璃管的作用是______________________________________________。
(4)以下收集NO气体的装置,合理的是________(填选项代号)。

(5)假设实验中12.8gCu全部溶解,需要通入标况下________LO2才能使NO全部溶于水。
(6)用金属铜制取硝酸铜,从节约原料和防止环境污染的角度考虑,下列4种方法中最好的是________(填“甲”、“乙”、“丙”或“丁”),理由是____________________________。
甲:铜+浓硝酸→硝酸铜
乙:铜+稀硝酸→硝酸铜
丙:铜+氯气→氯化铜;氯化铜+硝酸→硝酸铜
丁:铜+空气→氧化铜;氧化铜+硝酸→硝酸铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知酸性:H2SO3>H2CO3>HSO![]() >HCO
>HCO![]() ,某无色溶液Y中可能含有以下几种离子:Cl-、SO
,某无色溶液Y中可能含有以下几种离子:Cl-、SO![]() 、HCO
、HCO![]() 、HSO
、HSO![]() 、Fe3+、Ba2+、NH
、Fe3+、Ba2+、NH![]() 、Na+,溶液中阳离子浓度相同,为了确定其组成,某课题小组进行如下实验(假设气体均全部逸出、忽略H2O2的分解)
、Na+,溶液中阳离子浓度相同,为了确定其组成,某课题小组进行如下实验(假设气体均全部逸出、忽略H2O2的分解)
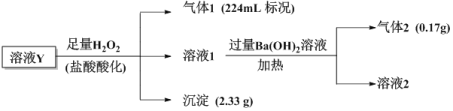
下列说法不正确的是
A.溶液1中一定不存在Fe3+、SO![]()
B.气体1为CO2气体
C.溶液Y中一定含有Cl-,且n(Cl-)=0.01mol
D.溶液Y中可能存在Na+,可取溶液1通过焰色反应实验验证
查看答案和解析>>
科目:高中化学 来源: 题型:
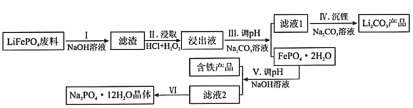
【题目】磷酸亚铁锂(LiFePO4)是目前使用量最多的一种锂电池电极材料,LiFePO4废料中(含Al、石墨)磷、铁、锂的综合回收工艺流程图:
已知:①![]() ,
,![]()
②常温下,![]() ,
,![]() ,
,![]()
(1)过程I“碱浸”的目的是____________,该过程发生反应的离子方程式为_________________。
(2)过程II“酸浸”加人双氧水的目的是_________________。
(3)①浸出液中存在大量![]() 、
、![]() 离子,从平衡移动角度解释过程Ⅲ得到磷酸铁晶体的原因_________________。
离子,从平衡移动角度解释过程Ⅲ得到磷酸铁晶体的原因_________________。
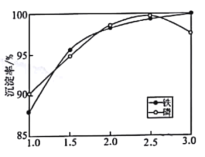
②一定条件下,探究了pH对磷酸铁沉淀的影响,结果如图所示。由图可知,过程Ⅲ应选取的最佳沉淀pH为____。随pH的增加,磷的沉淀率开始下降,而铁沉淀率未下降,分析原因为_________________。
(4)测得滤液1中c(Li+)=0.l5mol/L,某同学取该100mL滤液进行“沉锂”反应.加入50mlNa2CO3溶液却未见沉淀,若不考虑Na2CO3的水解和液体混合时的体积变化,则该同学加入的Na2CO3溶液最大浓度为c(Na2CO3)=_____________mol/L
(5)过程Ⅵ将滤液2________,________,经过滤、干燥后得Na3PO4·12H2O晶体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌-空气电池(原理如图)适宜用作城市电动车的动力电源。该电池放电时Zn转化为ZnO。该电池工作时下列说法正确的是
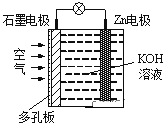
A. 氧气在石墨电极上发生氧化反应
B. 该电池的负极反应为Zn+H2O-2e- = ZnO+2H+
C. 该电池充电时应将Zn电极与电源负极相连
D. 该电池放电时OH-向石墨电极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于苯乙烯(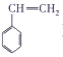 )有下列叙述,其中错误的是( )
)有下列叙述,其中错误的是( )
A.既可以与溴发生加成反应,又可以与溴发生取代反应
B.1mol苯乙烯最多可以与4mol氢气发生加成反应
C.苯乙烯分子中所有原子一定处于同一平面上
D.苯乙烯既可使酸性髙锰酸钾溶液褪色,又可使溴的四氯化碳溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是一种新型消毒剂的结构式,其中,Y、Z、W处于不同短周期、不同主族,X、W的简单离子核外电子排布相同,X的最外层电子数恰好等于Y、Z、W的最外层电子数之和,下列说法中正确的是( )

A.在元素周期表中,Y 位于 IVA 族
B.原子序数大小关系: Z > W > X > Y
C.W 元素被称为“国防金属”
D.电解熔融的氯化钠可得到 Z 的单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有两个实验小组的同学为探究过氧化钠与二氧化硫的反应,都用如图示的装置进行试验。通入二氧化硫气体,将带余烬的木条插入试管中,木条复燃。
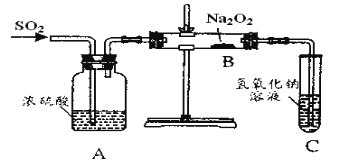
请回答下列问题:
(1)第一小组同学认为Na2O2与SO2反应生成的白色固体中含有Na2SO3和O2该反应的化学方程式为___。
(2)请设计一种实验方案证明Na2O2与SO2反应生成的白色固体中含有Na2SO3___。
(3)第二小组同学认为Na2O2与SO2反应除了生成Na2SO3和O2外还有Na2SO4生成。为检验是否有Na2SO4生成,他们设计了如下方案:
将B中反应后的固体溶解于水(再加BaCl2溶液)→白色沉淀→(加入稀硝酸)仍有部分白色沉淀不溶解,证明有Na2SO4生成。上述方案是否合理?___;请简要说明理由:__。
(4)在100mL混合溶液中,HNO3和H2SO4的物质的量浓度分别是0.4mol/L,0.1mol/L向该混合液中加入1.92g铜粉,加热待充分反应后,所得溶液中Cu2+的物质的量浓度是__(填选项字母)。
A.0.15 B.0.225 C.0.35 D.0.45
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氧化还原反应的说法正确的是
A.1mol Na2O2参与氧化还原反应,电子转移数一定为NA (NA为阿伏加德罗常数的值)
B.浓HCl和MnO2制氯气的反应中,参与反应的HCl中体现酸性和氧化性各占一半
C.VC可以防止亚铁离子转化成三价铁离子,主要原因是VC具有较强的还原性
D.NO2与水反应,氧化剂和还原剂的物质的量之比为2: 1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com