
| A、参加反应的硝酸是0.4mol |
| B、消耗氧气的体积为1.68 L |
| C、此反应过程中转移的电子为0.3 mol |
| D、混合气体中含NO21.12 L |
| 2.24L |
| 22.4L/mol |
| 1 |
| 2 |
| 2.24L |
| 22.4L/mol |
| 1 |
| 2 |
| 0.2mol |
| 4 |


科目:高中化学 来源: 题型:
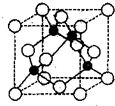 VIA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种化合价,含
VIA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种化合价,含查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 实验现象 | 解释或结论 |
| A | 把S02通入紫色石蕊试液中 | 紫色褪去 | SO2具有漂白性 |
B | 向NaOH溶液中滴加足量的MgCl2溶液, 然后再滴加足量的CuCl2溶液 | 先产生白色沉淀,然 后沉淀变蓝色 | KSP[Cu(OH)2]>KSP[Mg(OH)2] |
| C | 向某溶液中滴加KSCN溶液 | 溶液变红色 | 溶液中含有Fe3+ |
| D | 将充满N02的密闭玻璃球浸泡在热水中 | 红棕色变深 | 反应2NO2(g)?N2O4(g)的△H<0 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
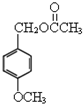 乙酸茴香酯具有花香和茴香香气,可作为配制食用香精的原料,其结构简式如图:
乙酸茴香酯具有花香和茴香香气,可作为配制食用香精的原料,其结构简式如图: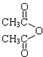 )反应制得.写出反应的化学方程式:
)反应制得.写出反应的化学方程式:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用食盐清洗热水瓶中的水垢 |
| B、漂白粉在空气中容易变质的原因是Ca(ClO)2见光分解 |
| C、加碘食盐,能使淀粉显蓝色 |
| D、氯水应避光保存,是因为HClO见光分解 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com