
| A. | Cl2具有很强的氧化性,在化学反应中只能作氧化剂 | |
| B. | 液氨汽化时要吸收大量的热,可用作制冷剂 | |
| C. | 二氧化硅不与强酸反应,可用石英器皿盛放氢氟酸 | |
| D. | SO2和Cl2都有漂白作用,将等物质的量的两种气体同时作用于潮湿的有色物质时,可增强漂白作用 |
分析 A.氯气与水反应生成氯化氢、次氯酸;
B.液氨汽化需要吸收大量的热,具有制冷作用;
C.二氧化硅与氢氟酸反应生成四氟化硅和水;
D.等物质的量的两种气体,反应生成硫酸和盐酸.
解答 解:A.氯气与水反应生成氯化氢、次氯酸,反应中氯气既做氧化剂又做还原剂,故A错误;
B.液氨汽化需要吸收大量的热,具有制冷作用,常用作制冷剂,故B正确;
C.二氧化硅与氢氟酸反应生成四氟化硅和水,所以氢氟酸能够腐蚀石英器皿,故C错误;
D.等物质的量的两种气体,反应生成硫酸和盐酸,盐酸与硫酸都不具有漂白性,故D错误;
故选;B.
点评 本题考查了元素化合物知识,明确氯气、液氨、二氧化硅、二氧化硫的性质是解题关键,题目难度不大.


 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:高中化学 来源: 题型:填空题
| 操作 | 现象 |
通入氯气至过量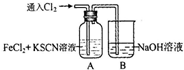 | Ⅰ、A中溶液变红 Ⅱ、稍后,溶液由红色变为黄色 |
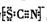 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素最高化合价:Al>Mg | B. | 金属性:Al>Mg | ||
| C. | 酸性:H2SO4>H3PO4 | D. | 稳定性:HF>HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学可以识别、改变和创造分子 | |
| B. | 金刚石常用作砂纸、砂轮的磨料 | |
| C. | 氧化铁常用作红色油漆和涂料 | |
| D. | 葡萄糖可用于合成补钙药物及维生素C(结构如图)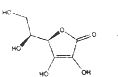 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
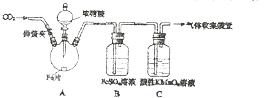 甲、乙两同学用如图所示装置进行实验,探究硝酸与铁反应的产物.
甲、乙两同学用如图所示装置进行实验,探究硝酸与铁反应的产物.| 实验操作 | 实验现象 |
| 打开弹簧夹,通入一段时间CO2,关闭弹簧夹. | / |
| 打开分液漏斗活塞,将浓硝酸缓慢滴入烧瓶中,关闭活塞. | 无明显现象. |
| 加热烧瓶,反应开始后停止加热. | ①A中有红棕色气体产生,一段时间后,气体颜色逐渐变浅; B中溶液变棕色; C中溶液紫色变浅. ②反应停止后,A中无固体剩余 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1a mol | B. | (0.1+a)mol | C. | (0.05+a)mol | D. | 2a mol |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
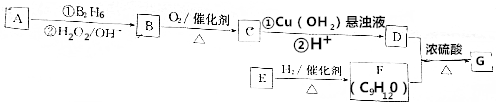
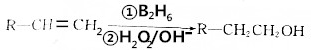
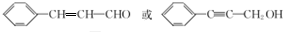 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4和Cl2光照发生取代反应 | |
| B. | 1,3丁二烯与等物质的量的溴发生反应 | |
| C. | CH3CH(OH)CH2CH3在浓硫酸作用下加热的反应 | |
| D. | 乙烯和氯化氢加成 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
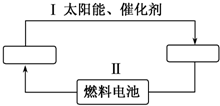 能源是21世纪极具发展前景的新能源之一,它既是绿色能源,又可循环使用.
能源是21世纪极具发展前景的新能源之一,它既是绿色能源,又可循环使用.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com