
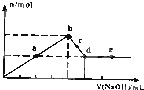
 向MgC12和A1C13的混合溶液中加入氢氧化钠溶液,所得沉淀的物质的量(n)与加入氢氧化钠溶液的体积(V)关系如图所示.则下列说法正确的是( )
向MgC12和A1C13的混合溶液中加入氢氧化钠溶液,所得沉淀的物质的量(n)与加入氢氧化钠溶液的体积(V)关系如图所示.则下列说法正确的是( )| A. | a、c两点沉淀物成份不相同,d、e两点沉淀物成份相同 | |
| B. | b点溶液的中c(Na+)=c(C1-) | |
| C. | b-c段与c-d段溶液中阴离子的物质的量相等 | |
| D. | 在d点,向溶液中加入少量盐酸,沉淀量将减少 |
分析 A.开始生成沉淀量到沉淀量最大,AlCl3和MgCl2的混合溶液与NaOH溶液,发生反应生成氢氧化铝、氢氧化镁沉淀,然后发生反应NaOH+Al(OH)3=NaAlO2+2H2O,氢氧化铝溶解,沉淀量不变时,氢氧化铝完全溶解,沉淀为氢氧化镁;
B.b点时沉淀量最大,AlCl3和MgCl2的混合溶液与NaOH溶液恰好反应,溶液中溶质为NaCl;
C.溶液中的阳离子为钠离子,阴离子为氯离子与偏铝酸根离子,都为1价离子,钠离子越多阴离子越多;
D.在d点沉淀量降低到最小,氢氧化铝完全溶解,沉淀为氢氧化镁,此时溶液为NaCl、NaAlO2溶液,滴加盐酸偏铝酸钠先反应.
解答 解:A.开始生成沉淀量到沉淀量最大,AlCl3和MgCl2的混合溶液与NaOH溶液,发生反应生成氢氧化铝、氢氧化镁沉淀,然后发生反应NaOH+Al(OH)3=NaAlO2+2H2O,a、c两点沉淀都是氢氧化铝与氢氧化镁,a、c两点沉淀物成份相同;在d点沉淀量降低到最小,氢氧化铝完全溶解,沉淀为氢氧化镁,故d、e两点沉淀都是氢氧化镁,故A错误;
B.b点时沉淀量最大,AlCl3和MgCl2的混合溶液与NaOH溶液恰好反应,溶液中溶质为NaCl,由电荷守恒可知溶液的中c(Na+)=c(C1-),故B正确;
C.溶液中的阳离子为钠离子,阴离子为氯离子与偏铝酸根离子,都为1价离子,c-d段溶液中钠离子更多,故c-d段溶液中阴离子多,故C错误;
D.在d点沉淀量降低到最小,氢氧化铝完全溶解,沉淀为氢氧化镁,此时溶液为NaCl、NaAlO2溶液,加入盐酸偏铝酸钠与盐酸反应生成氢氧化铝沉淀,沉淀量增大,故D错误;
故选B.
点评 本题考查了有关混合物反应的计算,题目难度不大,注意掌握质量守恒定律在化学计算中的应用方法,本题中明确反应后的溶质组成为解答关键,试题侧重考查学生的分析、理解能力.


科目:高中化学 来源: 题型:选择题
| A. | 治理拥堵,减少汽车尾气排放,大力发展清洁能源可以有效减少雾霾 | |
| B. | 铜的金属活动性比铝弱,可以用铜罐代替铝罐储运浓硝酸 | |
| C. | 光化学烟雾的形成和氮的氧化物有关,硫的氧化物是形成硫酸型酸雨的主要物质 | |
| D. | 硫化钠和亚硫酸钠的固体如果长期暴露在空气中容易变质 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
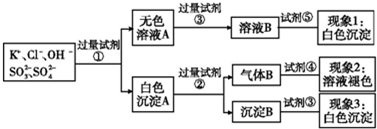
| A. | 试剂③是AgNO3溶液,试剂⑤是稀硝酸,现象1中白色沉淀是AgCl | |
| B. | 现象3中白色沉淀是BaSO4 | |
| C. | 产生现象2的离子方程式是:Br2+2H2O+SO2═4H++2Br-+SO42- | |
| D. | 试剂②是稀盐酸,试剂③是稀硝酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH和HAC | B. | KOH和HNO3 | C. | Ba(OH)2和H2SO4 | D. | NH3•H2O和HAC |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入铝粉能产生H2的溶液:Fe2+、NH4+、SO42-、NO3- | |
| B. | 室温下水电离出c(H+)=1×10-13mol/L的溶液:HCO3-、K+、SO42-、Cl- | |
| C. | 含大量Fe3+的溶液:NH4+、Na+、SCN-、Cl- | |
| D. | 使PH试纸呈深蓝色的溶液:Na+、K+、AlO2-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com