
| A. |  如图一个超氧化钾小晶胞中含有4个KO2 | |
| B. | 和K+距离相同且最近的O2-构成的多面体是正六面体 | |
| C. | 和K+距离相同且最近的K+有8个 | |
| D. | 和K+距离相同且最近的O2-共有8个 |
分析 A、根据均摊法进行计算;
B、以顶点上K+的为例,和K+距离相同且最近的O2-位于经过该顶点的棱边的中点;
C、以顶点上K+的为例,和K+距离相同且最近的K+-位于经过该顶点的面的面心上;
D、以顶点上K+的为例,和K+距离相同且最近的O2-位于经过该顶点的棱边的中点.
解答 解:A、K+位于晶胞棱心和体心,数目为12×$\frac{1}{4}$+1=4,O2-位于顶点和面心,数目为8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,即一个KO2晶胞中摊得的K+和O2-粒子数均为4个,故A正确;
B、与K+距离相等且最近的O2-共有6个,构成正八面体,K+位于正八面体中心,故B错误;
C、K+位于晶胞棱心,则被横平面、竖平面和正平面共有,且每一个平面有4个K+距离最近,共4×3=12个,故C错误;
D、K+位于晶胞棱心,与K+距离相等且最近的O2-位于顶点和面心,共有6个,故D错误;
故选A.
点评 本题考查晶胞计算和配位数,难度不大,要求学生有一定的空间想象能力.


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 上述三个反应都有单质生成,所以都是置换反应 | |
| B. | 氧化性由强到弱顺序为 KBrO3>KClO3>Cl2>Br2 | |
| C. | 反应②中还原剂与氧化剂的物质的量之比为6:1 | |
| D. | ③中lmol还原剂反应则氧化剂得到电子的物质的量为2mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 核内无中子的原子 | |
| B. | 价电子构型为3s23p1 | |
| C. | 最外层电子数等于倒数第三层上的电子数的原子 | |
| D. | N层上无电子,最外层上的电子数等于电子层数的原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.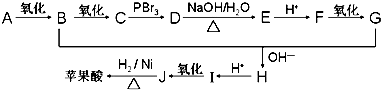


 +n HO-CH2CH2-OH$\stackrel{一定条件}{→}$
+n HO-CH2CH2-OH$\stackrel{一定条件}{→}$ +(2n-1)H2O
+(2n-1)H2O 、
、 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | A | B | C | D |
| 装置 | 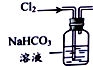 | 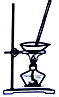 | 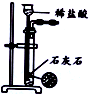 | 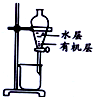 |
| 目的 | 除去Cl2中含有的少量HCl | 蒸发NaCl饱和溶液制备NaCl晶体 | 制取少量纯净的CO2气体 | 分离酒精和水的混合溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com