
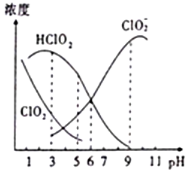
 织物漂白剂亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都只有漂白作用,但ClO2是有毒气体.25℃时,各组分浓度随pH变化情况如图所示(Cl-没有画出).下列说法不正确的是( )
织物漂白剂亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都只有漂白作用,但ClO2是有毒气体.25℃时,各组分浓度随pH变化情况如图所示(Cl-没有画出).下列说法不正确的是( )| A. | 25℃时,ClO2-的水解平衡常数Ka=10-6 | |
| B. | 在pH约为4.0~4.5范围内使用该漂白剂较好 | |
| C. | 25℃时,等浓度的HClO2溶液和NaClO2溶液等体积混合后,混合溶液中:c(HClO2)+c(H+)+c(Na+)═c(ClO2-)+2c(OH-) | |
| D. | 当pH=5时往NaClO2溶液中滴入稀氢氧化钠溶液,溶液中主要反应的离子方程式是:HClO2+OH-═H2O+ClO2- |
分析 A.ClO2-的水解平衡为:ClO2-+H2O?HClO2+OH-,平衡常数Kh=$\frac{c(HCl{O}_{2})c(O{H}^{-})}{c(Cl{{O}_{2}}^{-})}$,平衡常数只随温度变化,结合图象分析判断;
B.根据题意:HClO2和ClO2都具有漂白作用,结合图中HClO2和ClO2的浓度大小来确定使用该漂白剂的最佳pH;
C.依据电中性原则得出:c(H+)+c(Na+)=c(ClO2-)+c(OH-),依据物料守恒得出:2c(Na+)=c(ClO2-)+c(HClO2),据此解答即可;
D.图象分析可知当pH=5时溶液中主要是HClO2.
解答 解:A.ClO2-的水解平衡位:ClO2-+H2O?HClO2+OH-,平衡常数Kh=$\frac{c(HCl{O}_{2})c(O{H}^{-})}{c(Cl{{O}_{2}}^{-})}$,平衡常数只随温度变化,PH=6时,c(ClO2-)=c(HClO2),Kh=10-6,故A正确;
B.HClO2和ClO2都具有漂白作用,ClO2有毒,所以只能ClO2浓度越小越好,而同时HClO2浓度又必须大,所以选4-4.5,结合图中HClO2和ClO2的浓度,该漂白剂的最佳pH约为4,故B正确;
C.依据电中性原则得出:c(H+)+c(Na+)=c(ClO2-)+c(OH-) ①,依据物料守恒得出:2c(Na+)=c(ClO2-)+c(HClO2) ②,联立①②消去钠离子:c(HClO2)+2c(H+)=c(ClO2-)+2c(OH-),故C错误;
D.图象分析可知当pH=5时溶液中主要是HClO2,pH=5时往NaClO2溶液中滴入稀氢氧化钠溶液,溶液中主要反应的离子方程式是:HClO2+OH-═H2O+ClO2-,故D正确;
故选C.
点评 本题考查了酸碱混合的定性判断,题目难度中等,正确分析、理解题中信息及图象数据是解答本题关键,注意明确溶液酸碱性与溶液pH的关系.


科目:高中化学 来源: 题型:选择题
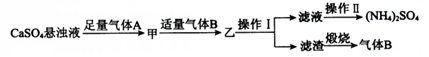
| A. | 气体B是NH3,可循环利用 | |
| B. | 操作Ⅰ中,所用的主要玻璃仪器为烧杯、玻璃棒、分液漏斗 | |
| C. | 操作Ⅱ中,可用蒸发结晶的方法得到纯净的(NH4)2SO4 | |
| D. | 整个过程的总反应方程式为CaSO4+CO2+2NH3+H2O═CaCO3↓+(NH4)2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溴被称为“海洋元素” | B. | 硅酸钠可作建筑行业的黏合剂 | ||
| C. | 碳酸钠可作治疗胃酸过多的药剂 | D. | 镁可用于制造信号和焰火 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
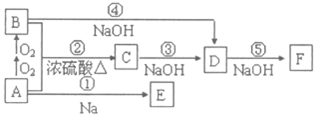
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 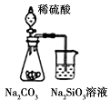 此装置可证明非金属性强弱:S>C>Si | |
| B. | 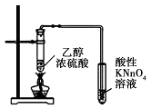 此装置可用于检验有乙烯生成 | |
| C. | 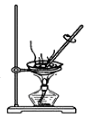 此装置可通过蒸干AlCl3饱和溶液制备AlCl3晶体 | |
| D. | 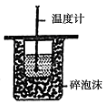 此装置可用来测定中和热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用乙醇萃取溴水中的溴单质 | |
| B. | 用干燥的pH试纸测定新制氯水的pH | |
| C. | 向NH4Cl溶液中滴加石蕊试液,溶液变红,证明NH4Cl发生了水解反应 | |
| D. | 向蒸馏水中滴加过量的饱和FeCl3溶液,并不断搅拌,制取Fe(OH)3胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 操 作 | 现 象 | 结 论 |
| A | 向蔗糖中加入浓硫酸 | 蔗糖变成疏松多孔的海绵状炭,并放出有剌激性气味的气体 | 浓硫酸具有脱水性和强氧化性 |
| B | 向盛有H2O2溶液的试管中加入几滴酸化的硫酸亚铁溶液 | 溶液变成棕黄色,一段时间后,溶液中出现气泡,随后有红褐色沉淀生成 | Fe2+催化H2O2分解产生O2;H2O2分解反应放热,促进Fe3+的水解平衡正向移动 |
| C | 铝片先用砂纸打磨,再加入 到浓硝酸中 | 无明显现象 | 浓硝酸具有强氧化性,常温下,铝被浓硝酸钝化 |
| D | 向等浓度的KC1、KI混合液中逐滴满加AgNO3溶液 | 先出现黄色沉淀 | Ksp(AgCl)>Ksp (AgI) |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 简单离子半径:W>Z>X | |
| B. | X、Y、Z都能与W组成离子化合物 | |
| C. | X、Y组成的化合物可与W单质反应 | |
| D. | Q是Z、W组成的化合物,1molQ中约含有6.02×1023个阴离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 按如图装置进行实验,下列推断正确的是( )
按如图装置进行实验,下列推断正确的是( )| 选项 | I中试剂 | II中试剂及现象 | 推断 |
| A | 氯化铵 | 酚酞溶液不变红色 | 氯化铵稳定 |
| B | 硫酸亚铁 | 品红溶液褪色 | FeSO4分解生成FeO和SO2 |
| C | 涂有石蜡油的碎瓷片 | 酸性高锰酸钾溶液褪色 | 石蜡油发生了化学变化 |
| D | 铁粉与水蒸气 | 肥皂水冒泡 | 铁粉与水蒸气发生了反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com