
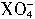 ��2X2����5Z2��8H2O����2M2����R2��2M3����2R������2R����Z2��R2��2Z�����ɴ��жϣ�����˵���д�����ǣ� ����
��2X2����5Z2��8H2O����2M2����R2��2M3����2R������2R����Z2��R2��2Z�����ɴ��жϣ�����˵���д�����ǣ� ����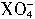 >Z2>R2>M3+
>Z2>R2>M3+ 
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��ͼ��ʾ����Ӧ����������ȥ����
��ͼ��ʾ����Ӧ����������ȥ����
| ||
| �� |
| ||
| �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������������ ���ͣ�013
��֪����������Һ�пɷ��������������ӷ�Ӧ��
 ��
��
�ɴ˿�ȷ�� ��
��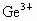 ��
�� �������ӵĻ�ԭ����ǿ������˳����
�������ӵĻ�ԭ����ǿ������˳����
[����]
A�� ��
�� ��
�� ����
B��
����
B�� ��
�� ��
��
C�� ��
�� ��
�� ����
D��
����
D�� ��
�� ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�013
��֪����������Һ�пɷ��������������ӷ�Ӧ��
 ��
��
�ɴ˿�ȷ�� ��
�� ��
�� �������ӵĻ�ԭ����ǿ������˳����
�������ӵĻ�ԭ����ǿ������˳����
[����]
A�� ��
�� ��
�� ����
B��
����
B�� ��
�� ��
��
C�� ��
�� ��
�� ����
D��
����
D�� ��
�� ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010-2011ѧ�����ʡ��������У������ѧ����ĩ���ԣ����ۣ���ѧ���� ���ͣ������
A��B��C��D�Ƕ�����Ԫ���γɵ��������嵥�ʡ�E��F��Ϊ���壬��FΪ����ɫ���йص�ת����ϵ����ͼ��ʾ����Ӧ����������ȥ����

��ش��������⣺
��1��D�Ļ�ѧʽΪ ��
��2����Ӧ�۵����ӷ���ʽΪ ��
��3��Y��E��һ�������¿ɷ�Ӧ����B��Z������һ������ʵ������ķ�Ӧ��������E�Ի�������Ⱦ���÷�Ӧ�Ļ�ѧ����ʽΪ ��
��4��0.1mol/L��X��Һ��0.1mol/L��Y��Һ�������ϣ���Һ��________�ԣ�����ᡱ��������С�������Һ�и�����Ũ�ȴ�С��ϵΪ��_______________________
��5��������0.1mol/L��Y��Һ��c(H+)/c(OH-)=110��8������������ȷ���ǣ� ��
A������Һ��pH=11��
B������Һ�е����ʵ������������Ũ��0.1mol/L
C������Һ��ˮ�������c(H+)��c(OH-)�˻�Ϊ110��22
D�� pH=3��������ҺV1 L���0.1mol/L��Y��ҺV2 L���,�������ҺpH=7����:V1>V2
E����pH=11��Y��Һ��ˮϡ��100����pHֵΪ9��
��6��������E��һ����������һ������������пɷ�����������ԭ��Ӧ����������������ѹǿ��С��ԭ����2/3����д���÷�Ӧ�Ļ�ѧ����ʽ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com