
| 有机物A | 有机物B | 有机物C | 有机物D |
| ①可用于果实催熟 ②比例模型为  | ①由C、H两种元素组成 ②球棍模型为  | ①生活中常见的液态有机物,分子中碳原子数与有机物A相同 ②能与Na反应,但不能与NaOH反应 | ①相对分子质量比有机物C大14 ②能由有机物C氧化生成 |
分析 由表格中的信息可知,A为CH2=CH2,由B的球棍模型可知,B为苯,C为生活中常见的液态有机物,分子中碳原子数与有机物A相同,能与Na反应,但不能与NaOH反应,说明含有羟基,但不含羧基,应为CH3CH2OH,D由C氧化生成,相对分子质量比有机物C大14,应为CH3COOH,然后结合有机物的性质来解答该题.
解答 解:(1)A为CH2=CH2,分子式为C2H4,故答案为:C2H4;
(2)a.苯性质稳定,与高锰酸钾不反应,不能使酸性KMnO4溶液褪色,故a错误;
b.A、B都为平面形结构,则分子中所有的原子在同一平面内,故b正确;
c.A、B含氢量不同,等质量的A、B完全燃烧,消耗氧气的量不相同,故c错误;
d.苯不含有官能团碳碳双键,故d错误.
故答案为:b;
(3)C为乙醇,对应的同分异构体为CH3OCH3,故答案为:CH3OCH3;
(4)乙酸、乙醇在浓硫酸作用下加热可发生酯化反应生成乙酸乙酯,反应的化学方程式为CH3COOH+CH3CH2OH $?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O,
n(CH3COOH)=$\frac{5g}{60g/mol}$=$\frac{5}{60}$mol,n(CH3COOCH2CH3)=$\frac{4.4g}{88g/mol}$=0.05mol,则D的转化率为$\frac{0.05}{\frac{5}{60}}×100%$=60%.
故答案为:CH3COOH+CH3CH2OH $?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O;60%.
点评 本题考查有机物的推断,为高频考点,侧重考查学生的分析能力,把握官能团与性质的关系为解答的关键,题目着重于性质、结构推断物质的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | Cu2S是唯一的还原产物 | |
| B. | 反应中的氧化剂只有CuSO4 | |
| C. | 被氧化与被还原硫元素的质量比为7:3 | |
| D. | 若以该反应为原理设计原电池,电池的正极为石墨棒,负极是吸附有FeS2粉末的多孔石墨电极,电解质溶液为CuSO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
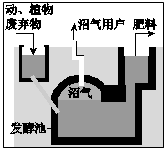 阅读下文,回答问题.
阅读下文,回答问题. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 采取低碳、节俭的生活方式 | |
| B. | 严禁排放未经处理的有毒工业废水 | |
| C. | 经常使用一次性筷子、塑料袋等 | |
| D. | 按照规定对生活废弃物进行分类放置 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 (1)a图中的图1表示10mL量筒中液面的位置,A与B,B与C刻度间相差1mL,如果刻度A为4,量简中液体的体积是3.2mL.
(1)a图中的图1表示10mL量筒中液面的位置,A与B,B与C刻度间相差1mL,如果刻度A为4,量简中液体的体积是3.2mL.| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(Fe3+)=1 xl0-5 mol•L-1 | |
| B. | 加水稀释,平衡①向右移动 | |
| C. | 加入等体积0.2 mol•L-1KSCN溶液,溶液变为血红色 | |
| D. | 加入等体积0.2 mol•L-1CaCl2溶液,可产生沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 装置①常用于分离互不相溶的液体混合物 | |
| B. | 装置②用于吸收氨气,能够防止倒吸 | |
| C. | 以NH4Cl和熟石灰为原料,装置③可制备少量NH3 | |
| D. | 装置④a口进气可收集Cl2、NO等气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com