
设NA为阿伏加德罗常数的数值,下列说法正确的是
A.18gH2O含有l0NA个质子
B.1mol甲苯含有6NA个C-H键
C.标准状况下,22.4L氨水含有NA个NH3分子
D.56g铁片投入足量浓H2SO4中生成NA个SO2分子
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2017届重庆市高三上定时训练(七)化学试卷(解析版) 题型:选择题
二氧化氮存在下列平衡:2NO2(g) N2O4(g)(放热反应),在测定NO2的相对分子质量时,下列条件较为适宜的是
N2O4(g)(放热反应),在测定NO2的相对分子质量时,下列条件较为适宜的是
A.温度130℃、压强3.03×105Pa B.温度25℃、压强1.01×105Pa
C.温度0℃、压强5.05×104Pa D.温度130℃、压强5.05×104Pa
查看答案和解析>>
科目:高中化学 来源:2017届山西省高三上学期10月月考化学试卷(解析版) 题型:选择题
800℃在2L密闭容器内,充入0.020molNO与0.010mol的O2,发生反应2NO(g)+O2(g)  2NO2(g) n(NO)随时间的变化如表:
2NO2(g) n(NO)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO) (mol) | 0.020 | 0.010 | 0.009 | 0.008 | 0.008 | 0.008 |

A.a线表示NO2的变化趋势,则0~2s内v(NO2)=0.006mol/(L·s)
B.800℃时,该反应的平衡常数K=1125L/mol
C.能使该反应的反应速率增大,且平衡向正方向移动的措施是及时分离出NO2
D.已知:K300℃>K350℃,则该反应时吸热反应
查看答案和解析>>
科目:高中化学 来源:2017届湖南省长沙市高三上月考二化学试卷(解析版) 题型:选择题
为除去括号内的杂质,下列各选顶中所选用的试剂或方法不正确的是
A.Na2CO3溶液(NaHCO3),选用适量的NaOH溶液
B.NaHCO3溶液(Na2CO3),应通入过量的CO2气体
C.Na2O2粉末(Na2O),将混合物在空气中加热
D.Na2CO3溶液(Na2SO4),加入适量的Ba(OH)2溶液,过滤
查看答案和解析>>
科目:高中化学 来源:2017届广西省高三上学期10月月考化学试卷(解析版) 题型:填空题
铈、铬、钛、镍虽不是中学阶段常见的金属元素,但在工业生产中有着重要作用。
(1)二氧化铈 (CeO2)在平板电视显示屏中有着重要应用。CeO2在稀硫酸和H2O2的作用下可生成Ce3+,写出该反应的化学方程式 ,CeO2在该反应中作__________剂。
(2)自然界中Cr主要以+3价和+6价存在,+6价的Cr能引起细胞的突变。现用亚硫酸钠溶液与0.1mol K2Cr2O7反应,将其+6价的Cr完全还原为+3价的铬,则消耗1mol/L亚硫酸钠溶液的体积为 L。
(3)钛(Ti)被誉为“二十一世纪的金属”,工业上在550℃时用钠与四氯化钛反应可制得钛,该反应的化学方程式是 。
(4)NiSO4·xH2O是一种绿色易溶于水的晶体,广泛用于镀镍、电池等,可由电镀废渣(除镍外,还含有铜、锌、铁等元素)为原料获得.操作步骤如下:
①向滤液Ⅰ中加入FeS是为了除去Cu2+、Zn2+等杂质(已知溶解度FeS>CuS)。请写出除去Cu2+的离子方程式 。
②对滤液Ⅱ先加H2O2再调pH。加H2O2的目的是 ,调pH的目的是 。
③滤液Ⅲ溶质的主要成分是NiSO4,加Na2CO3过滤后,再加适量稀硫酸溶解又生成NiSO4,这两步操作的目的是 。
查看答案和解析>>
科目:高中化学 来源:2017届广西省高三上学期10月月考化学试卷(解析版) 题型:选择题
设NA为阿伏加罗常数的值,下列说法正确的是
A.298K 101kPa时,22.4L CO2所含的原子数为3NA
B.1mol Cl2与足量的Fe完全反应,转移的电子数为2NA
C.0.5mol C2H2和C6H6的气态混合物中所含原子总数为2NA
D.2L 1mol/L的盐酸中所含HCl分子数约为2NA
查看答案和解析>>
科目:高中化学 来源:2017届河北邯郸市高三上学期第二次月考化学试卷(解析版) 题型:选择题
有一瓶Na2SO3溶液,可能部分被氧化,某同学进行如下实验:取少量此溶液,滴入Ba(NO3)2溶液产生白色沉淀,再加入足量稀HCl,充分振荡后仍有白色沉淀,对此实验下列结论正确的是( )
A.加HCl后的不溶沉淀一定为BaSO4
B.此溶液中Na2SO3已部分氧化
C.加入Ba(NO3)2溶液生成的沉淀一定含BaSO4
D.此样品未被氧化
查看答案和解析>>
科目:高中化学 来源:2017届浙江省高三上学期10月月考化学试卷(解析版) 题型:实验题
重铬酸钾是一种常见的强氧化剂。实验室以精选铬铁矿(主要成分可表示为FeO.Cr2O3,还含有SiO2、Al2O3等杂质)为原料制备重铬酸钾晶体(K2Cr2O7,式量294)的流程如下:
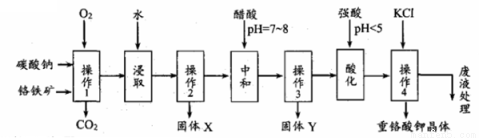
请回答下列问题:
⑴操作1中发生的反应有:
4FeO·Cr2O3 + 8Na2CO3 + 7O2 = 8Na2CrO4 + 2Fe2O3 + 8CO2↑
Na2CO3 + Al2O3 = 2NaAlO2 + CO2↑
Na2CO3 + SiO2 = Na2SiO3 + CO2↑
该步骤在常温下的反应速率较慢,为使反应速率增大,可采取的措施是 (写出两条)
⑵固体Y中主要含有 。(填写化学式)
⑶酸化步骤使含铬物质发生了转化为_________,请写出离子反应方程式 。
⑷操作4中的化学反应在溶液中能发生的可能理由是 ,获得晶体的操作依次是:加入KCl固体,在水浴上加热浓缩至 ,冷却结晶,抽滤、洗涤、干燥。
⑸通过下列实验可测定产品中重铬酸钾的质量分数:
称取重铬酸钾试样1.470g,用100mL容量瓶配制成溶液。移取25.00mL溶液于碘量瓶中,加入适量稀硫酸和足量碘化钾(铬的还原产物为Cr3+),放于暗处5min。然后加入一定量的水,加入淀粉指示剂,用0.1500mol/L Na2S2O3标准溶液滴定,共消耗标准液36.00mL。滴定时发生的反应的离子方程式为:
I2 + 2S2O32- = 2I- + S4O62-
则所测定产品中重铬酸钾的纯度为 。
⑹有关上述实验过程中涉及的部分实验操作的描述,正确的是 。
A.粗产品若要进一步提纯,可以采用重结晶的方法
B.配制溶液时,用托盘天平称取试样后,一般经溶解、转移(含洗涤)、定容等步骤,配制成100mL溶液
C.滴定时,当最后一滴标准溶液滴入时,溶液变为蓝色,且半分钟内不变色,可判断滴定终点
D.滴定终点时俯视读数,测定结果偏低
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com