
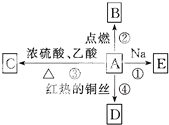
 A是化学实验室中最常见的有机物,能进行如图所示的多种反应.
A是化学实验室中最常见的有机物,能进行如图所示的多种反应. CH3COOCH2CH3+H2O;反应④2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
CH3COOCH2CH3+H2O;反应④2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O. 分析 A能与钠反应、能被催化氧化、能和乙酸发生酯化反应,且A是化学实验室中最常见的有机物,则A为CH3CH2OH,乙醇和钠反应生成乙醇钠,则E为CH3CH2ONa,A被催化氧化生成D,D为CH3CHO、A和乙酸发生酯化反应生成C,C为CH3COOCH2CH3,乙醇燃烧生成二氧化碳和水,据此分析解答.
解答 解:A能与钠反应、能被催化氧化、能和乙酸发生酯化反应,且A是化学实验室中最常见的有机物,则A为CH3CH2OH,乙醇和钠反应生成乙醇钠,则E为CH3CH2ONa,A被催化氧化生成D,D为CH3CHO、A和乙酸发生酯化反应生成C,C为CH3COOCH2CH3,乙醇燃烧生成二氧化碳和水,
(1)A是乙醇,C是乙酸乙酯,分子式为C4H8O2,
故答案为:乙醇;C4H8O2;
(2)反应③是乙醇和乙酸的酯化反应,反应方程式为CH3COOH+CH3CH2OH  CH3COOCH2CH3+H2O,
CH3COOCH2CH3+H2O,
反应④是乙醇的催化氧化反应,反应方程式为2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O,
故答案为:CH3COOH+CH3CH2OH  CH3COOCH2CH3+H2O;2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
CH3COOCH2CH3+H2O;2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断能力,根据反应条件结合官能团及其性质关系进行推断,题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
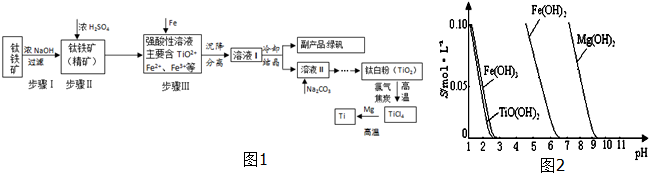
| TiCl4 | Mg | MgCl2 | Ti | |
| 熔点/℃ | -25.0 | 648.8 | 714 | 1667 |
| 沸点/℃ | 136.4 | 1090 | 1412 | 3287 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
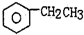 (g)$\stackrel{560℃}{?}$
(g)$\stackrel{560℃}{?}$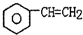 (g)+H2(g)△H<0
(g)+H2(g)△H<0| A. | 加入适当催化剂,可以提高乙苯的转化率 | |
| B. | 在保持体积一定的条件下,充入较多的乙苯,可以提高乙本的转化率 | |
| C. | 在加入乙苯至达到平衡过程中,混合气体的平均相对分子质量不变 | |
| D. | 仅从平衡移动的角度分析,工业生产苯乙稀选择恒压条件优于恒容条件 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| T/K | 298 | 398 | 498 |
| 平衡常数K | 51 | K1 | K2 |
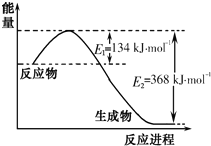
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③ | B. | ③④ | C. | ①②③ | D. | ③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子半径 Z>X | B. | 最外层电子数 Z>Y | ||
| C. | 金属性 Z>X | D. | 原子半径 Z>Y |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
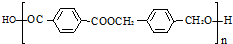 的路线:
的路线: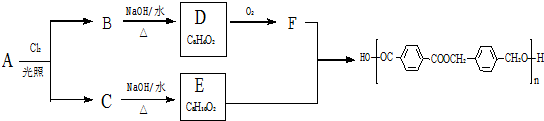
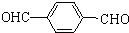 ,由B生成D的反应过程中生成的不稳定中间体的结构简式是
,由B生成D的反应过程中生成的不稳定中间体的结构简式是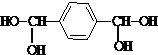 ,该中间体生成D的反应类型为消去反应.
,该中间体生成D的反应类型为消去反应.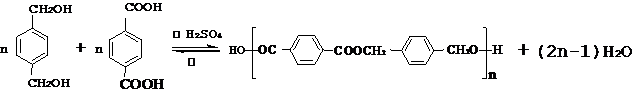 ,反应类型为缩聚反应.与E具有相同官能团的含苯环的同分异构体有(写结构简式)
,反应类型为缩聚反应.与E具有相同官能团的含苯环的同分异构体有(写结构简式)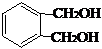 、
、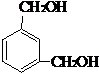 、
、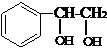 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com