
CO2�������г����Ļ�����֮һ���������繤ҵ���õķ�չ���˿ڵľ�����ȫ����Դ���ż�������������Խ��Խ���ص����⣬�����CO2�������о����ۺ������������ӡ�
���ڴ��������£����ɼ״���CO2ֱ�Ӻϳ�̼�������(DMC)��CO2 + 2CH3OH �� CO(OCH3)2 + H2O�����״�ת����ͨ�����ᳬ��1%��������Լ�÷�Ӧ����ҵ������Ҫԭ��ij�о�С���������������������£�ͨ���о��¶ȡ���Ӧʱ�䡢���������ֱ��ת����(TON)��Ӱ�������۴����Ĵ�Ч�������㹫ʽΪ��TON��ת���ļ״������ʵ���/���������ʵ�����
��1�����ݷ�Ӧ�¶ȶ�TON��Ӱ��ͼ����ͬʱ���ڲⶨ�����жϸ÷�Ӧ���ʱ��H________0�����������������������������____________________________________��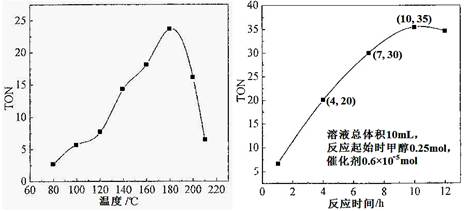
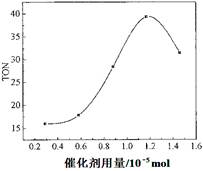
��2�����ݷ�Ӧʱ���TON��Ӱ��ͼ����ͼ������֪��Һ�����10mL����Ӧ��ʼʱ�״�0.25mol������0.6��10��5 mol��������¶��£�4��7 h��DMC��ƽ����Ӧ���ʣ�________��
��3�����ݸ��о�С���ʵ�鼰����������TON��Ӱ��ͼ��������ͼ�����ж�����˵����ȷ���� ��
A���ɼ״���CO2ֱ�Ӻϳ�DMC���������ü״���Ӱ�컷������������CO2 ת��Ϊ��Դ������Դѭ�����úͻ����������涼������Ҫ����
B. �ڷ�Ӧ��ϵ�����Ӻ��ʵ���ˮ��������߸÷�Ӧ��TON
C. ��������������1.2��10��5 molʱ�����Ŵ������������ӣ��״���ƽ��ת�����������
D. ��������������1.2��10��5 molʱ�����Ŵ�������������DMC�IJ��ʷ��������½�
��.��������ڵ�CO2����˳���ų������������ж���������Һ���Ե������������������ҺpH��Ӱ�죬����ѪҺ����Ҫͨ��̼�����λ�����ϵ(H2CO3/HCO3-)ά��pH�ȶ�����֪��������ѪҺ����������ʱ��H2CO3��һ�����볣��Ka1=10-6.1��c(HCO3-):c(H2CO3)��20:1��lg2=0.3��
(4)��������ݿ������������ѪҺ��pH________(����һλС��)��
(5)��������ѪҺ��H2CO3��HCO3-��OH-��H+������Ũ���ɴ�С��ϵΪ�� ��
(6)���������ᡢ�����ѪҺ��ʱ��ѪҺpH�仯������ԭ�������������������������� ��
��1������ ������ͬ�ķ�Ӧʱ�䣬�¶Ƚϵ�ʱ����Ӧδ�ﵽƽ�⣻�¶Ƚϸ�ʱ����Ӧ�Ѵﵽƽ�⣬�����¶����ߣ�TON��С����ƽ�������ƶ���˵���÷�Ӧ���� ��2��1��10-3 mol��L-1��h-1
��3��AB (4) 7.4 (5)c(HCO3-)��c(H2CO3)��c(OH-)��c(H+)
(6)�����������ѪҺ��ʱ��HCO3-����H+������Ӧ��ά��ѪҺ��pH�ȶ��������������ѪҺ��ʱ��H2CO3����OH_������Ӧ��ά��ѪҺ��pH�ȶ�
���������������1������ͼ���֪��������ͬ�ķ�Ӧʱ�䣬�¶Ƚϵ�ʱ����Ӧδ�ﵽƽ�⣻�¶Ƚϸ�ʱ����Ӧ�Ѵﵽƽ�⣬�����¶����ߣ�TON��С����ƽ�������ƶ���˵���÷�Ӧ���ȡ�
��2������ͼ���֪��4��7 h��DMC�仯��Ϊ30��20��10�������TON��ת���ļ״������ʵ���/���������ʵ�����֪��ת���ļ״����ʵ�����0.6��10��5 mol��10��6��10��5 mol����Ũ����6��10��5 mol��0.01L��6��10��3 mol/L������DMC��Ũ����3��10��3 mol/L������4��7 h��DMC��ƽ����Ӧ���ʣ�3��10��3 mol/L��3h��1��10-3 mol��L-1��h-1��
��3��A���ɼ״���CO2ֱ�Ӻϳ�DMC���������ü״���Ӱ�컷������������CO2 ת��Ϊ��Դ������Դѭ�����úͻ����������涼������Ҫ���壬A��ȷ��B���ڷ�Ӧ��ϵ�����Ӻ��ʵ���ˮ�������Խ���������ˮ������Ũ�ȣ���ʹƽ��������Ӧ������У��״���ת����������˽���߸÷�Ӧ��TON��B��ȷ��C������TON��ת���ļ״������ʵ���/���������ʵ�����֪��TON��״�ת�������Լ������������й�ϵ�����Ե�������������1.2��10��5 molʱ�����Ŵ������������ӣ��״���ƽ��ת���ʲ�һ������ߣ�C����ȷ��D���������ܸı�ƽ��״̬�����DMC�IJ����������ϵ��D����ȷ����ѡAB��
��4��Ka��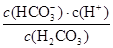 ��Ka=10-6.1mol?L-1������ѪҺ��c��HCO3-����c��H2CO3����20��1����c��H+��=10-7.4mol?L-1����pH��7.4��
��Ka=10-6.1mol?L-1������ѪҺ��c��HCO3-����c��H2CO3����20��1����c��H+��=10-7.4mol?L-1����pH��7.4��
��5�����ݣ�4���з�����֪��������ѪҺ�Լ��ԣ�c(OH-)��c(H+)����֪Ka��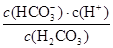 ��10-6.1��ѪҺ��ƷpHΪ7.4����c��H+��=10-7.4mol/L������
��10-6.1��ѪҺ��ƷpHΪ7.4����c��H+��=10-7.4mol/L������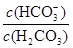 ��10?6.1��10?7.4��101.3�����ѪҺ��H2CO3��HCO3-��OH-��H+������Ũ���ɴ�С��ϵΪc(HCO3-)��c(H2CO3)��c(OH-)��c(H+)��
��10?6.1��10?7.4��101.3�����ѪҺ��H2CO3��HCO3-��OH-��H+������Ũ���ɴ�С��ϵΪc(HCO3-)��c(H2CO3)��c(OH-)��c(H+)��
��6��ѪҺ�д���H2CO3 HCO3-+H+ƽ�⣬������ǿʱ��ѪҺ��������Ũ��������ƽ�������ƶ���������ǿʱ����������Ũ������ƽ�������ƶ�����˿���ά��ѪҺ��pH�ȶ���
HCO3-+H+ƽ�⣬������ǿʱ��ѪҺ��������Ũ��������ƽ�������ƶ���������ǿʱ����������Ũ������ƽ�������ƶ�����˿���ά��ѪҺ��pH�ȶ���
���㣺������������Է�Ӧ���ʺ�ƽ��״̬��Ӱ�졢���淴Ӧ�����Լ���Һ��pH���������Ũ�ȴ�С�Ƚ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��6�֣�ijѧϰС����������ϡ����ķ�Ӧ�����С�̽��Ӱ�컯ѧ��Ӧ�������ء���ʵ�顣������±���
| ʵ�� ��� | ��������/g | ���� ��̬ | V(H2SO4) /mL | c(H2SO4) /mol��L-1 | ��Ӧǰ��Һ ���¶�/�� | ������ȫ�� ʧ��ʱ��/s |
| 1 | 0.10 | Ƭ״ | 50 | 0.8 | 20 | 200 |
| 2 | 0.10 | ��״ | 50 | 0.8 | 20 | 25 |
| 3 | 0.10 | Ƭ״ | 50 | 1.0 | 20 | 125 |
| 4 | 0.10 | Ƭ״ | 50 | 1.0 | 35 | 50 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��14�֣���̼����(��Ҫָ����CO2)�ڽ������������ŷ��о�����Ҫ�����á�ĿǰNH3��(NH4)2CO3�Ѿ���������ҵ��̼����������CO2�ɷ������¿��淴Ӧ��
��Ӧ��2NH3(l)��H2O(l)��CO2(g)  (NH4)2CO3(aq) ��H1
(NH4)2CO3(aq) ��H1
��Ӧ��NH3(l)��H2O(l)��CO2(g)  NH4HCO3(aq) ��H2
NH4HCO3(aq) ��H2
��Ӧ��(NH4)2CO3(aq)��H2O(l)��CO2(g)  2NH4HCO3(aq) ��H3
2NH4HCO3(aq) ��H3
��ش��������⣺
(1)��H3�릤H1����H2֮��Ĺ�ϵ�ǣ���H3�� ��
(2) ��Ӧ��Ļ�ѧƽ�ⳣ������ʽΪ ��
(3)Ϊ�о��¶ȶ�(NH4)2CO3����CO2Ч�ʵ�Ӱ�죬��ij�¶�T1�£���һ������(NH4)2CO3��Һ�����ܱ������У�������һ������CO2����(�õ�����Ϊϡ�ͼ�)����tʱ�̣����������CO2�����Ũ�ȡ�Ȼ��ֱ����¶�ΪT2��T3��T4��T5�£�����������ʼʵ���������䣬�ظ�����ʵ�飬������ͬʱ����CO2����Ũ�ȣ��õ�����ͼ(��ͼ1)����
�٦�H3 0(�����������������)��
����T1��T2��T4��T5�����¶����䣬������CO2����Ũ�ȳ�����ͼ1��ʾ�ı仯���ƣ���ԭ����
��
�۷�Ӧ�����¶�ΪT1ʱ����ҺpH��ʱ��仯������������ͼ2��ʾ����ʱ�䵽��t1ʱ�����÷�Ӧ��ϵ�¶�Ѹ��������T2����ά�ָ��¶ȡ����ڸ�ͼ�л���t1ʱ�̺���Һ��pH�仯���������ߡ�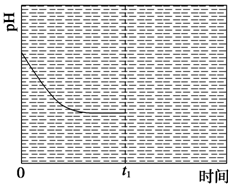
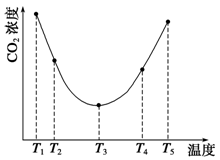
ͼ1 ͼ2
(4)���÷�Ӧ��CO2����(NH4)2CO3��ʼŨ�Ⱥ����ȷ��������£����CO2�������Ĵ�ʩ��
��
(5)����������Ҳ������ΪCO2��������� ��
| A��NH4Cl | B��Na2CO3 | C��HOCH2CH2OH | D��HOCH2CH2NH2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��17�֣��о����������������ڴ����к������ӵ������ʱ���漰���·�Ӧ��
2NO2��g��+NaCl��s��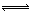 NaNO3��s��+ClNO��g�� K1 ?H < 0 ��I��
NaNO3��s��+ClNO��g�� K1 ?H < 0 ��I��
2NO��g��+Cl2��g��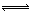 2ClNO��g�� K2 ?H < 0 ��II��
2ClNO��g�� K2 ?H < 0 ��II��
��1��4NO2��g��+2NaCl��s��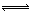 2NaNO3��s��+2NO��g��+Cl2��g����ƽ�ⳣ��K= ����K1��K2��ʾ����
2NaNO3��s��+2NO��g��+Cl2��g����ƽ�ⳣ��K= ����K1��K2��ʾ����
��2��Ϊ�о���ͬ�����Է�Ӧ��II����Ӱ�죬�ں��������£���2L�����ܱ������м���0.2mol NO��0.1mol Cl2��10minʱ��Ӧ��II���ﵽƽ�⡣���10min��v��ClNO��=7.5��10-3mol?L-1?min-1����ƽ���n��Cl2��= mol��NO��ת���ʧ�1= �������������ֲ��䣬��Ӧ��II���ں�ѹ�����½��У�ƽ��ʱNO��ת���ʧ�2 ��1���>����<����=������ƽ�ⳣ��K2 ���������С�����䡱����ҪʹK2��С���ɲ��õĴ�ʩ�� ��
��3��ʵ���ҿ���NaOH��Һ����NO2����ӦΪ2NO2+2NaOH=NaNO3+NaNO2+H2O����0.2mol NaOH��ˮ��Һ��0.2mol NO2ǡ����ȫ��Ӧ��1L��ҺA����ҺBΪ0.1mol?L?1��CH3COONa��Һ��������Һ��c��NO3?����c��NO2-����c��CH3COO?���ɴ�С��˳��Ϊ ������֪HNO2�ĵ��볣��Ka=7.1��10-4mol?L?1��CH3COOH�ĵ��볣��K a=1.7��10-5mol?L?1����ʹ��ҺA����ҺB��pH��ȵķ����� ��
a������ҺA�м�����ˮ b������ҺA�м�����NaOH
c������ҺB�м�����ˮ d������ҺB�м�����NaOH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
(17��)���û�ѧ��Ӧԭ���о�̼�Ļ����������Ҫ���塣
��1��������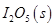 �����ڼ��CO����Ӧԭ��Ϊ��
�����ڼ��CO����Ӧԭ��Ϊ��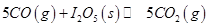
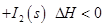 ����2L�ܱ������м�������
����2L�ܱ������м�������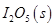 ����ͨ��1molCO��CO2���������
����ͨ��1molCO��CO2���������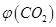 ��ʱ��ı仯����ͼ��ʾ��
��ʱ��ı仯����ͼ��ʾ��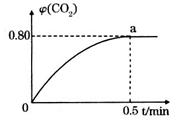
��0��0.5min�ڵ�ƽ����Ӧ����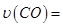 _____________��
_____________��
�ڱ����¶Ⱥ�������䣬����ʼ����CO(g)�����ʵ�����ԭ����2����������˵����ȷ����____________(�����)��
a������I2������Ϊԭ����2��
b����������ƽ��Ħ����������
c���ﵽƽ���ʱ��Ϊԭ����2��
d�����������ܶȲ���
�۷�Ӧ��a��ʱ��������������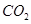 ���������
���������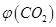 ���ɲ�ȡ�Ĵ�ʩΪ____________��
���ɲ�ȡ�Ĵ�ʩΪ____________��
��2����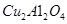 Ϊ���������Խ�
Ϊ���������Խ�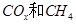 �Ļ������ֱ��ת��Ϊ���ᡣ
�Ļ������ֱ��ת��Ϊ���ᡣ
�����÷�Ӧ��ԭ��������Ϊ100������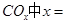 ______________��
______________��
����25���£���pH=a������������Һ��pH=b�Ĵ�����Һ�������ϣ�������Һǡ����ȫ��Ӧ����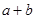 ________14(�>������<����=��)�����¶��´���ĵ��볣��K=__________(�ú�a��b��ʽ�ӱ�ʾ)��
________14(�>������<����=��)�����¶��´���ĵ��볣��K=__________(�ú�a��b��ʽ�ӱ�ʾ)��
��3�����÷�Ӧ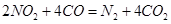 ���Դ�������β���������÷�Ӧ���Ϊԭ��أ�������Na2O������ʣ��������缫��ӦʽΪ________________________________��
���Դ�������β���������÷�Ӧ���Ϊԭ��أ�������Na2O������ʣ��������缫��ӦʽΪ________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��6�֣���6molA�����2molB������2L�ܱ������л�ϲ���һ�������·�����Ӧ��3A��g��+B��g�� xC��g��+2D��g��������5min��Ӧ�ﵽƽ��״̬�������ڵ�ѹǿ��С����֪D��ƽ����Ӧ����Ϊ0.2mol/��L?min��,����д���пհף�
xC��g��+2D��g��������5min��Ӧ�ﵽƽ��״̬�������ڵ�ѹǿ��С����֪D��ƽ����Ӧ����Ϊ0.2mol/��L?min��,����д���пհף�
��x����ֵΪ �� ��A��ƽ����Ӧ����Ϊ �� ��5minʱB��ת����Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
(14��)
�������ڹ�ҵ�������й㷺����;��
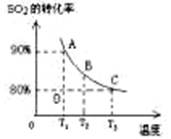
��1�����ڿ��淴Ӧ2SO2(g)��O2(g)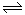 2SO3(g) ��H��0�������о�Ŀ�ĺ�ͼʾ�������
2SO3(g) ��H��0�������о�Ŀ�ĺ�ͼʾ�������
������ţ�
| ��� | A | B | C | D |
| Ŀ�� | ѹǿ��ƽ���Ӱ�� | �¶ȶ�ת���ʵ�Ӱ�� | ����O2Ũ�ȶ����ʵ�Ӱ�� | Ũ�ȶ�ƽ�ⳣ����Ӱ�� |
| ͼʾ | 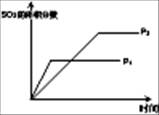 |  | 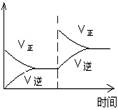 | 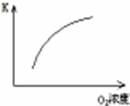 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
(15��)������ˮ��������Ⱦ��������Ҫ���⡣��ˮ�и�Ԫ����Cr2O72-��CrO42-��ʽ���ڣ������������������ǣ�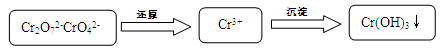
��1���������ʹCrO42-ת��ΪCr2O72-�� 2CrO42- + 2H+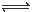 Cr2O72- + H2O
Cr2O72- + H2O
��������pH=1��Һ��Cr2O72-Ũ��Ϊ0��1 mol?L-1��Cr2O72-Ũ����CrO42-Ũ�ȵ�10�����û�ѧƽ�ⳣ��K= ��
��2�����۸��Ķ��Դ�Լ�����۸���100������������ԭ������������Һ��ͨSO2��Cr2O72-��ԭ����Ӧ�����ӷ���ʽΪ �������ټӼCr3+��������֪������Ksp��Cr(OH)3�� =10-32,Ҫʹc(Cr3+)���͵�10-5mol?L-1����Һ��pHӦ���ߵ� ��
��3����ԭ�������õ�������Fe2+��Cr2O72-��ԭΪCr3+�����װ�����õĵ缫������̼������Ƭ��������Ƭ����ֱ����Դ�� ����
��4��Cr(OH)3Ϊ��ɫճ�Գ�����������Al(OH)3����������������ǿ����Һ��Cr(OH)3����ϡ����Ļ�ѧ����ʽΪ ����100��00mL 0��1000 mol?L-1CrCl3��Һ�μ�1��000mol?L-1NaOH��Һ, �뻭�����ɳ��������ʵ��������NaOH��Һ����Ĺ�ϵͼ: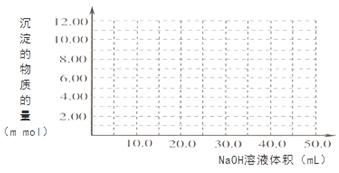
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��������ЧӦ����Դ��ȱ�����⣬��ν��ʹ����е�CO2���������Կ������ã������˸�����ձ����ӡ�Ŀǰ��ҵ����һ�ַ�������CO2����ȼ�ϼ״���һ�������·�����Ӧ��CO2(g)��3H2(g)  CH3OH(g)��H2O(g)���÷�Ӧ�������仯��ͼ��ʾ��
CH3OH(g)��H2O(g)���÷�Ӧ�������仯��ͼ��ʾ��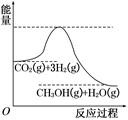
(1)������Ӧƽ�ⳣ��K�ı���ʽΪ ���¶Ƚ��ͣ�ƽ�ⳣ��K (����������䡱��С��)��
(2)�����Ϊ2 L���ܱ������У�����1 mol CO2��3 mol H2�����CO2�����ʵ�����ʱ��仯���±���ʾ���ӷ�Ӧ��ʼ��5 minĩ��������Ũ�ȱ仯��ʾ��ƽ����Ӧ����v(H2)�� ��
| t/min | 0 | 2 | 5 | 10 | 15 |
| n(CO2)/mol | 1 | 0.75 | 0.5 | 0.25 | 0.25 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com