
| A、FeSO4酸性溶液暴露在空气中:4Fe2++O2+4H+═4Fe3++2H2O |
| B、过量石灰水与碳酸氢钙反应:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O |
| C、向Na[Al(OH)4]溶液中通入过量CO2:[Al(OH)4]-+CO2═Al(OH)3↓+HCO3- |
| D、在强碱性溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:4OH-+3ClO-+2Fe(OH)3═2FeO42-+3Cl-+5H2O |


科目:高中化学 来源: 题型:
| A、氯气可使湿润的红布条退色,所以氯气具有漂白性 |
| B、在通常情况下,氯气可以和任何金属直接化合 |
| C、氯气没有漂白性,但通入品红溶液中,品红会退色 |
| D、氯气是黄绿色气体,闻其气味时要小心将集气瓶放在鼻孔下直接闻 |
查看答案和解析>>
科目:高中化学 来源: 题型:
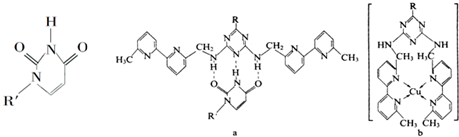
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,11.2L苯所含分子数为0.5NA |
| B、pH=2、体积为1L的醋酸溶液中含醋酸分子的数目为0.01NA |
| C、标准状况下,11.2LNH3和9gH2O所含电子的数目均为5NA |
| D、1mol Cu 发生氧化反应时一定失去2NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、100mL3mol/LKClO3溶液 |
| B、75mL2.5mol/LMgCl2溶液 |
| C、150mL3mol/LKCl溶液 |
| D、25mL2mol/LAlCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 混合物 | 碱 | 盐 | 碱性氧化物 | 酸性氧化物 | |
| A | 液氧 | 苛性钠 | 胆矾 | 氧化铁 | 二氧化碳 |
| B | 盐酸 | 烧碱 | 食盐 | 氧化钠 | 一氧化碳 |
| C | 84消毒液 | 纯碱 | 石灰石 | 氨气 | 水 |
| D | 漂白粉 | 熟石灰 | 苏打 | 生石灰 | 二氧化硫 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
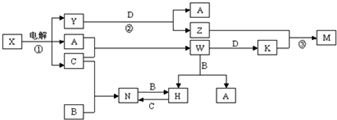
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com