
| A. |  除去CO中的CO2 | B. | 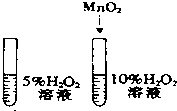 探究二氧化锰对反应速率的影响 | ||
| C. | 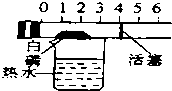 探究空气中氧气的含量 | D. |  探究溶解性的影响因素 |
分析 A.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质;
B.探究二氧化锰对反应速率的影响,可用控制变量法,控制其它条件相同;
C.白磷燃烧产生固体,使注射器内的气压变小;
D.探究影响物质溶解性的因素,可用控制变量法,控制其它条件相同.
解答 解:A.一氧化碳与氧化铁反应生成铁和二氧化碳,反而会把原物质除去,不符合除杂原则,故A错误;
B.探究二氧化锰对反应速率的影响,需要控制过氧化氢溶液的浓度相同,一个加入二氧化锰,一个不加二氧化锰,图中过氧化氢溶液的浓度不同,故B错误;
C.白磷燃烧产生固体,使注射器内的气压变小,根据气体变化的体积差可以计算氧气的含量,故C正确;
D.探究溶解性的影响因素时,两支试管内都应放碘,一支试管内放水,一支试管内放酒精,看溶剂的影响;或通过放入溶剂相同,溶质不同来验证溶质的影响,不能达到目的,故D错误.
故选C.
点评 本题考查化学实验方案的评价,难度不是很大,化学实验方案的设计是考查学生能力的主要类型,同时也是实验教与学难点,在具体设计时要对其原理透彻理解,可根据物质的物理性质和化学性质结合实验目的进行分析判断.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:填空题
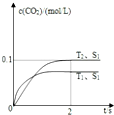 重庆市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5μm的悬浮颗粒物),其主要来源为燃煤、机动车尾气等.因此,对PM2.5、SO2、NOx等进行研究具有重要意义.请回答下列问题:
重庆市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5μm的悬浮颗粒物),其主要来源为燃煤、机动车尾气等.因此,对PM2.5、SO2、NOx等进行研究具有重要意义.请回答下列问题:| 离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol•L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化性:PdCl2>CO2 | |
| B. | 生成22.4LCO2时,转移的电子为2mo1 | |
| C. | 反应中PdCl2被氧化 | |
| D. | CO气体只有在高温下才能表现还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2和CO2都是酸性氧化物,都能与强碱溶浓反应 | |
| B. | SiO2和CO2都能溶于水且与水反应生成相应的酸 | |
| C. | 工艺师利用HF溶液刻蚀石英制作艺术品 | |
| D. | 除去SiO2中混有的CaCO3可加入适量的稀盐酸,然后过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 工艺流程如图.
工艺流程如图.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子核中有7个中子的碳原子:12C | |
| B. | 明矾的电离方程式是:KAl(SO4)2•12H2O═K++Al3++2SO42-+12H2O | |
| C. | K+结构示意图: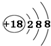 | |
| D. | Ba(OH)2与H2SO4反应的化学方程式是:Ba(OH)2+H2SO4═BaSO4↓+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com