
稀的醋酸溶液中存在平衡CH3COOH⇌CH3COO﹣+H+(正方向吸热),要使溶液中c(H+)减小,下列操作正确的是( )
|
| A. | 溶液中加入氢氧化钠固体 | B. | 溶液中通入HCl气体 |
|
| C. | 使醋酸溶液的温度升高 | D. | 加入纯醋酸 |
考点:
弱电解质在水溶液中的电离平衡.
专题:
电离平衡与溶液的pH专题.
分析:
根据题意知,要使溶液中c(H+)减小,则加入的物质要和H+反应或降低温度抑制醋酸电离,据此分析解答.
解答:
A.向溶液中加入氢氧化钠固体,氢氧化钠和氢离子反应生成水,所以能减少c(H+),故A正确;
B.向溶液中通入氯化氢气体,盐酸中含有氢离子,虽然能抑制醋酸电离,但溶液中增多的氢离子远远大于抑制醋酸电离的氢离子,所以溶液中c(H+)增大,故B错误;
C.升高温度,促进醋酸的电离,溶液中氢离子浓度增大,故C错误;
D.加入纯醋酸,平衡向正反应方向移动,导致溶液中氢离子浓度增大,故D错误.
故选A.
点评:
本题考查了影响弱电解质电离的因素,难度不大,注意:如果加入含有相同离子的物质就抑制其电离,如果加入和弱电解质电离的离子发生反应的物质就促进其电离.


科目:高中化学 来源: 题型:
下列反应属于氧化还原反应的是( )
|
| A. | CaO+H2O=Ca(OH)2 | B. | NaCl+AgNO3=NaNO3+AgCl↓ |
|
| C. | H 2CO3=H2O+CO2↑ | D. | H2+CuO=Cu+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各反应达到化学平衡后,加压能使化学平衡向逆反应方向移动的是( )
|
| A. | 2NO2⇌N2O4 | B. | C(s)+CO2⇌2CO | C. | N2+3H2⇌2NH3 | D. | H2S⇌H2+S(s) |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列热化学方程式中△H的绝对值能表示可燃物的燃烧热的是( )
|
| A. | H2(g)+Cl2(g)=2HCl(g);△H=﹣184.6kJ/mol |
|
| B. | CH4(g)+2O2(g)=CO2(g)+2H2O(g);△H=﹣802.3kJ/mol |
|
| C. | 2H2(g)+O2(g)=2H2O(l);△H=﹣571.6kJ/mol |
|
| D. | CO(g)+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
如图是关于反应A2(g)+3B2(g)⇌2C(g)△H<0的平衡移动图形,影响平衡移动的原因是( )

|
| A. | 升高温度,同时加压 |
|
| B. | 降低温度,同时减压 |
|
| C. | 增大反应物浓度,同时减小生成物浓度 |
|
| D. | 增大反应物浓度,同时使用催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应A2(g)+2B2(g)⇌2AB2(g)(正反应放热),下列说法正确的( )
|
| A. | 升高温度,正向反应速率减小,逆向反应速率增加 |
|
| B. | 升高温度有利于反应速率增加,从而缩短达到平衡的时间 |
|
| C. | 达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动 |
|
| D. | 达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
250℃和1.01×105Pa时,反应 2N2O5(g)=4NO2(g)+O2(g);△H=+56.76kJ•mol﹣1,自发进行的原因是( )
|
| A. | 是吸热反应 | B. | 是放热反应 |
|
| C. | 是熵减少的反应 | D. | 熵增大效应大于焓变效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,在容积固定的密闭容器中进行可逆反应:2NO2⇌2NO+O2,达到平衡的标志是( )
①相同时间内,氧气的生成速率为n mol•L﹣1•s﹣1,NO2的生成速率为2n mol•L﹣1•s﹣1
②单位时间内生成n mol O2的同时生成2n mol的NO
③混合气体的颜色不再变化
④混合气体的密度保持不变
⑤混合气体的平均相对分子质量不再改变
⑥压强不随时间变化而变化.
|
| A. | ①③⑤⑥ | B. | ②③⑤ | C. | ①③④ | D. | ①②③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
高氯酸三碳酰肼合镍{[Ni(CHZ)3](ClO4)2 }是一种新型的起爆药。
(1)Ni2+基态核外电子排布式为 。
(2)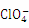 的空间构型是 ;与
的空间构型是 ;与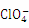 互为等电子体的一种分子为 (填化学式)。
互为等电子体的一种分子为 (填化学式)。
(3)化学式中CHZ为碳酰肼,组成为CO(N2H3)2,碳酰肼中碳原子的杂化轨道类型为 ;1molCO(N2H3)2分子中含有σ键数目为 。
(4)高氯酸三碳酰肼合镍可由NiO、高氯酸及碳酰肼化合而成。NiO的晶胞结构如图所示,晶胞中含有的Ni2+数目为a,Ni2+的配位数为b,NiO晶体中每个镍离子距离最近的镍离子数目为c,则a∶b∶c= 。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com